Глицин - Glycine
| |||
| |||
| Атаулар | |||
|---|---|---|---|
| Басқа атаулар 2-аминоэтан қышқылы, гликолол | |||
| Идентификаторлар | |||
3D моделі (JSmol ) | |||
| Қысқартулар | Gly, G | ||
| Чеби | |||
| ЧЕМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA ақпарат картасы | 100.000.248 | ||
| EC нөмірі |
| ||
| KEGG | |||
PubChem CID | |||
| UNII | |||
CompTox бақылау тақтасы (EPA) | |||
| |||
| |||
| Қасиеттері | |||
| C2H5NO2 | |||
| Молярлық масса | 75.067 г · моль−1 | ||
| Сыртқы түрі | Ақ қатты | ||
| Тығыздығы | 1.1607 г / см3[2] | ||
| Еру нүктесі | 233 ° C (451 ° F; 506 K) (ыдырау) | ||
| 24,99 г / 100 мл (25 ° C)[3] | |||
| Ерігіштік | ериді пиридин ішінде аз ериді этанол ерімейді эфир | ||
| Қышқылдық (бҚа) | 2,34 (карбоксил), 9,6 (амин)[4] | ||
| -40.3·10−6 см3/ моль | |||
| Фармакология | |||
| B05CX03 (ДДСҰ) | |||
| Қауіпті жағдайлар | |||
| Қауіпсіздік туралы ақпарат парағы | Қараңыз: деректер беті | ||
| Өлтіретін доза немесе концентрация (LD, LC): | |||
LD50 (медианалық доза ) | 2600 мг / кг (тышқан, ауызша) | ||
| Қосымша мәліметтер парағы | |||
| Сыну көрсеткіші (n), Диэлектрикалық тұрақты (εр) және т.б. | |||
Термодинамика деректер | Фазалық тәртіп қатты-сұйық-газ | ||
| Ультрафиолет, IR, NMR, ХАНЫМ | |||
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |||
| Infobox сілтемелері | |||
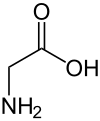
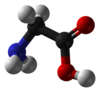
Глицин (белгі) Gly немесе G;[5] /ˈɡлaɪсменn/)[6] болып табылады амин қышқылы жалғыз бар сутегі атом оның бүйір тізбек. Бұл ең қарапайым амин қышқылы (содан бері) көмір қышқылы тұрақсыз), бірге химиялық формула NH2 ‐CH2 ‐COOH. Глицин - бірі протеиногенді амин қышқылдары. Бұл кодталған барлық кодондар GG-ден (GGU, GGC, GGA, GGG) бастап. Глицин түзілудің ажырамас бөлігі болып табылады альфа-спирттер ықшам формасының арқасында екінші протеин құрылымында. Сол себепті, бұл ең көп мөлшерде болатын амин қышқылы коллаген үштік спираль. Глицин сонымен қатар ингибитор болып табылады нейротрансмиттер - жұлынның бөлінуіне кедергі (мысалы, а. кезінде) Тетани Clostridium инфекция) тудыруы мүмкін спастикалық тежелмеген бұлшықет жиырылуына байланысты паралич.
Глицин - түссіз, тәтті дәмді кристалды қатты зат. Бұл жалғыз ахирал протеиногенді амин қышқылы. Ол сыйып кетуі мүмкін гидрофильді немесе гидрофобты қоршаған орта, бір ғана сутегі атомының ең аз бүйірлік тізбегіне байланысты. Ацил радикалды болып табылады глицил.
Тарих және этимология
Глицинді 1820 жылы француз химигі ашты Анри Браконно ол гидролизденгенде желатин оны қайнату арқылы күкірт қышқылы.[7] Ол бастапқыда оны «желатин қант» деп атады,[8][9] бірақ француз химигі Жан-Батист Буссинго құрамында азот бар екенін көрсетті.[10] Американдық ғалым Эбен Нортон Хорсфорд, содан кейін неміс химигінің студенті Юстус фон Либиг, «гликоколл» атауын ұсынды;[11][12] дегенмен Швед химик Берзелиус қарапайым «глицин» атауын ұсынды.[13][14] Атауы Грек сөз γλυκύς «тәтті дәм»[15] (бұл префикстермен де байланысты глико- және глюко-, сияқты гликопротеин және глюкоза ). 1858 жылы француз химигі Огюст Каурс глициннің ан амин туралы сірке қышқылы.[16]
Өндіріс
Глицинді гидролизденген ақуыздан бөліп алуға болатындығына қарамастан, оны өнеркәсіптік өндіріс үшін қолданбайды, өйткені оны химиялық синтездеу арқылы ыңғайлы етіп жасауға болады.[17] Екі негізгі процесс - аминация хлорсірке қышқылы бірге аммиак, глицин беру және аммоний хлориді,[18] және Strecker аминқышқылдарының синтезі,[19] бұл АҚШ пен Жапониядағы негізгі синтетикалық әдіс.[20] 15 мыңға жуық тонна осылайша жыл сайын шығарылады.[21]
Глицин синтезіндегі қоспа ретінде де бөлінеді EDTA, аммиактың қосымша өнімі реакцияларынан туындайды.[22]
Химиялық реакциялар
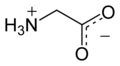
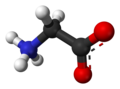
Оның қышқылды-негіздік қасиеттері ең маңызды. Сулы ерітіндіде глициннің өзі болады амфотериялық: төмен рН кезінде молекула р-мен протондануы мүмкінҚа шамамен 2,4 және жоғары рН кезінде ол протонды р-мен жоғалтадыҚа шамамен 9,6 (б. дәл мәндеріҚа температураға және иондық күшке байланысты).
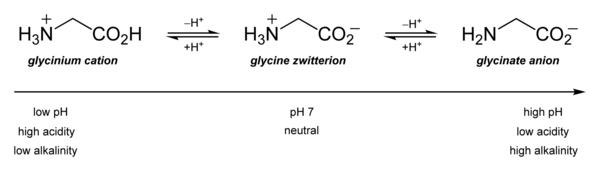
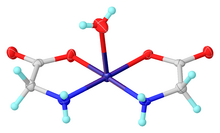
Глицин функциясы а битант лиганд көптеген металл иондары үшін Әдеттегі кешен - Cu (глицинат)2, яғни Cu (H2NCH2CO2)2, бұл цисада да, транс изомерлерде де бар.
Екіфункционалды молекула ретінде глицин көптеген реактивтермен әрекеттеседі. Оларды N-орталықтандырылған және карбоксилат-орталық реакциялар деп жіктеуге болады.
Амин күтілген реакцияларға ұшырайды. Қышқыл хлоридтермен бірге амидокарбон қышқылын алады гиппур қышқылы[23] және ацетилгликин.[24] Бірге азот қышқылы, біреуін алады гликоль қышқылы (ван Слайкты анықтау ). Метил йодидімен амин беру үшін кватерленеді бетаин, табиғи өнім:
- H
3N+
CH
2COO−
+ 3 CH3I → (CH
3)
3N+
CH
2COO−
+ 3 HI
Глицин түзілуінен басталатын пептидтер беру үшін өзімен бірге конденсацияланады глицилгликин:
- 2 H
3N+
CH
2COO−
→ H
3N+
CH
2КОНХЧ
2COO−
+ H2O
Глицин немесе глицилглициннің пиролизі 2,5- құрайдыдикетопиперазин, циклдік диамид.
Метаболизм
Биосинтез
Глицин жоқ адамның тамақтануы үшін маңызды, өйткені ол аминқышқылынан организмде биосинтезделеді серин, ол өз кезегінде алынған 3-фосфоглицерат, бірақ глицин биосинтезінің метаболизм қабілеті коллаген синтезіне деген қажеттілікті қанағаттандырмайды.[25] Көптеген организмдерде фермент сериндік гидроксиметилтрансфераза бұл трансформацияны кофактор арқылы катализдейді пиридоксалды фосфат:[26]
- серин + тетрагидрофолат → глицин + N5,N10-Тетрагидрофолат метилені + H2O
Бауырында омыртқалылар, глицин синтезі катализдейді глицин синтазы (глицинді бөлу ферменті деп те атайды). Бұл түрлендіру оңай қайтымды:[26]
- CO2 + NH+
4 + N5,N10-Тетрагидрофолат метилені + NADH + H+ ⇌ Глицин + тетрагидрофолат + НАД+
Деградация
Глицин үш жол арқылы ыдырайды. Жануарлар мен өсімдіктердегі басым жол жоғарыда аталған глицинт синтаза жолының кері бағыты болып табылады. Бұл тұрғыда қатысатын ферменттер жүйесі әдетте деп аталады глицинді бөлу жүйесі:[26]
- Глицин + тетрагидрофолат + NAD+ ⇌ CO2 + NH+
4 + N5,N10-Тетрагидрофолат метилені + НАДХ + H+
Екінші жолда глицин екі сатыда ыдырайды. Бірінші қадам - сериннен гидроксиметил трансферазасы бар сериннен глицин биосинтезінің кері әрекеті. Содан кейін серинге айналады пируват арқылы серинді дегидратаза.[26]
Оның ыдырауының үшінші жолында глицин айналады глиоксилат арқылы D-аминқышқылының оксидазасы. Содан кейін глиоксилат бауырмен тотығады лактатдегидрогеназа дейін оксалат NAD-да+- тәуелді реакция.[26]
Глициннің жартылай шығарылу кезеңі және оның организмнен шығарылуы дозаға байланысты айтарлықтай өзгереді.[27] Бір зерттеуде жартылай шығарылу кезеңі 0,5 пен 4,0 сағат аралығында өзгерді.[27]
Глицин фолийге бағытталған антибиотиктерге өте сезімтал және антибиотик инъекциясының бір минутында қандағы глицин деңгейі қатты төмендейді. Кейбір антибиотиктер енгізілгеннен кейін бірнеше минут ішінде глициннің 90% -дан астамын жоғалтуы мүмкін.[28]
Физиологиялық функция
Глициннің негізгі функциясы а белоктардың ізашары. Көптеген ақуыздар тек аз мөлшерде глицинді қосады, бұл ерекше жағдай коллаген, құрамында коллагеннің спираль құрылымын қалыптастырудағы мезгіл-мезгіл қайталанатын рөліне байланысты шамамен 35% глицин бар гидроксипролин.[26][29] Ішінде генетикалық код, глицин барлығымен кодталған кодондар GG бастап, атап айтқанда GGU, GGC, GGA және GGG.
Биосинтетикалық аралық ретінде
Жоғарыда эукариоттар, δ-аминолевулин қышқылы, үшін басты ізашары порфириндер, глициннен биосинтезделеді сукцинил-КоА фермент арқылы ALA синтезі. Глицин орталық Ц-ны қамтамасыз етеді2Барлығының бірлігі пуриндер.[26]
Нейротрансмиттер ретінде
Глицин ингибитор болып табылады нейротрансмиттер ішінде орталық жүйке жүйесі, әсіресе жұлын, ми діңі, және торлы қабық. Қашан глицин рецепторлары қосылды, хлорид ионотропты рецепторлар арқылы нейронға еніп, ан тудырады ингибиторлық постсинапстық потенциал (IPSP). Стрихнин ионотропты глицин рецепторларының күшті антагонисті болып табылады бикукуллин әлсіз. Глицин қажет бірлескен агонист бірге глутамат үшін NMDA рецепторлары. Жұлындағы глициннің ингибиторлық рөлінен айырмашылығы, бұл мінез-құлық (NMDA ) глутаматергиялық қоздырғыш болып табылатын рецепторлар.[30] The LD50 егеуқұйрықтарда глицин 7930 мг / кг, (ауызша),[31] және бұл әдетте гиперқозғыштықтың салдарынан өлімге әкеледі.
Қолданады
АҚШ-та глицин әдетте екі сұрыпта сатылады: Америка Құрама Штаттарының фармакопеясы («USP»), және техникалық дәрежесі. USP маркалы сатылым АҚШ-тың глицин нарығының шамамен 80 - 85 пайызын құрайды. Егер USP стандартынан жоғары тазалық қажет болса, мысалы ішілік инъекциялар, глициннің қымбат фармацевтикалық маркасын қолдануға болады. USP стандартының стандарттарына сәйкес келуі мүмкін немесе сәйкес келмейтін техникалық глицин өнеркәсіптік салаларда қолдану үшін төмен бағамен сатылады, мысалы, металдарды кешендеу және әрлеу кезінде агент ретінде.[32]
Жануарларға және адамдарға арналған тағамдар
Глицин инфузиядан басқа тағамдық құндылығы бойынша тағамдарда кеңінен қолданылмайды. Оның орнына глициннің тағамдық химиядағы маңызы хош иістендіргіш болып табылады. Бұл сахариннің дәмін анықтайтын жұмсақ тәтті. Оның консерванттық қасиеттері бар, мүмкін бұл металл иондарының құрамына кіреді. Металл глицинат кешендері, мысалы. мыс (II) глицинаты жануарларға арналған азықтық қоспалар ретінде қолданылады.[21]
Химиялық шикізат
Глицин - бұл әртүрлі химиялық өнімдерді синтездеудегі аралық зат. Ол өндірісте қолданылады гербицидтер глифосат,[34] ипродион, глифосин, имипротрин, және эглиназин.[21] Ол дәрі-дәрмектің аралық құралы ретінде қолданылады тиамфеникол.[дәйексөз қажет ]
Зертханалық зерттеу
Глицин - кейбір ерітінділердің маңызды құрамдас бөлігі SDS-БЕТ ақуызды талдау әдісі. Ол буферлік агент ретінде қызмет етеді, рН деңгейін сақтайды және электрофорез кезінде сынаманың зақымдануын болдырмайды. Глицин ақуызды таңбалайтын антиденелерді жою үшін қолданылады Western blot SDS-PAGE гельінен алынған көптеген ақуыздарды зерттеуге мүмкіндік беретін мембраналар. Бұл дәл сол үлгіден көбірек мәліметтер алуға мүмкіндік береді, бұл мәліметтердің сенімділігін арттырады, сынаманы өңдеу көлемін азайтады және қажетті сынамалар санын азайтады. Бұл процесс аршу деп аталады.
Ғарышта болу
Глициннің жердің сыртында болуы 2004 жылы алынған үлгілерді талдау негізінде 2009 жылы расталды НАСА ғарыш кемесі Жұлдыз кометадан Жабайы 2 содан кейін жерге оралды. Глицин бұрын анықталған Мурчисон метеориті 1970 ж.[35] Кометалық глициннің ашылуы теориясын күшейтті панспермия, бұл өмірдің «құрылыс материалдары» бүкіл Әлемде кең таралған деп мәлімдейді.[36] 2016 жылы 67P кометасында глицинді анықтау / Чурюмов-Герасименко Розетта ғарыш кемесі жарияланды.[37]
Глицинді сырттан анықтау күн жүйесі ішінде жұлдызаралық орта пікірталасқа түсті.[38] 2008 жылы Макс Планк атындағы Радио астрономия институты глицинге ұқсас молекуланың спектрлік сызықтарын ашты аминоацетонитрил ішінде Үлкен молекула Геймат, шоқжұлдыздағы галактикалық орталықтың жанындағы алып газ бұлты Стрелец.[39]
Эволюция
Әр түрлі типтегі деректерді қолдана отырып жүргізілген бірнеше тәуелсіз эволюциялық зерттеулер глициннің ерте генетикалық кодты құрайтын аминқышқылдарының тобына жататындығын дәлелдеді.[40][41][42][43] Мысалға, күрделілігі төмен аймақтар проте-пептидтерге ұқсас болуы мүмкін (белоктарда) генетикалық код глицинмен өте байытылған.[43]
Тамақ өнімдерінде болуы
| Азық-түлік | г / 100г |
|---|---|
| Тіскебасарлар, шошқа терілері | 11.04 |
| кунжут дәндері ұн (аз май) | 3.43 |
| Сусындар, ақуыз ұнтағы (соя негізделген) | 2.37 |
| Ішінара майсыздандырылған тұқымдар, мақсары тұқымдарының ұны | 2.22 |
| Ет, бизон, сиыр еті және басқалары (әр түрлі бөліктер) | 1.5-2.0 |
| Желатинді десерттер | 1.96 |
| Тұқымдар, асқабақ және сквош дәндер | 1.82 |
| Түркия, барлық сыныптар, арқа, ет және тері | 1.79 |
| Тауық еті, бройлер немесе қуырғыш, ет және тері | 1.74 |
| Шошқа еті, ұнтақталған, 96% майсыз / 4% май, пісірілген, ұсақталады | 1.71 |
| Бекон және сиыр таяқшалары | 1.64 |
| Жержаңғақ | 1.63 |
| Шаян тәрізділер, тікенді омар | 1.59 |
| Дәмдеуіштер, қыша тұқымы, жер | 1.59 |
| Салами | 1.55 |
| Жаңғақтар, сары май, кептірілген | 1.51 |
| Балық, лосось, қызғылт, консервіленген, құрғатылған қатты заттар | 1.42 |
| Бадам | 1.42 |
| Балық, скумбрия | 0.93 |
| Дәнді дақылдар жеуге дайын, гранола, үй | 0.81 |
| Пияз, (пиязшық және төменгі жапырақ бөлігі), мұздатып кептіріңіз | 0.7 |
| Ірімшік, пармезан (және басқалары), үгітілген | 0.56 |
| Соя, жасыл, пісірілген, қайнатылған, құрғатылған, тұзсыз | 0.51 |
| Нан, ақуыз (глютенді қосады) | 0.47 |
| Жұмыртқа, тұтас, пісірілген, қуырылған | 0.47 |
| Бұршақ, ақ, піскен тұқымдар, пісірілген, қайнатылған, тұзбен | 0.38 |
| Жасымық, піскен тұқымдар, пісірілген, қайнатылған, тұзбен | 0.37 |
Сондай-ақ қараңыз
Әдебиеттер тізімі
- ^ Мерк индексі: Химиялық, дәрілік және биологиялық энциклопедия (11-ші басылым), Мерк, 1989, ISBN 091191028X, 4386.
- ^ Химия және физика бойынша анықтамалық, CRC Press, 59-шы басылым, 1978 ж
- ^ «Ерігіштік және тығыздық». Prowl.rockefeller.edu. Алынған 2013-11-13.
- ^ Доусон, RMC және т.б., Биохимиялық зерттеулерге арналған мәліметтер, Оксфорд, Кларендон Пресс, 1959 ж.
- ^ «Аминқышқылдары мен пептидтердің номенклатурасы мен символикасы». IUPAC-IUB биохимиялық номенклатура бойынша бірлескен комиссия. 1983. мұрағатталған түпнұсқа 2008 жылғы 9 қазанда. Алынған 5 наурыз 2018.
- ^ «Глицин | Оксфорд сөздіктері бойынша глициннің ағылшынша анықтамасы».
- ^ Плиммер, Р.Х.А. (1912) [1908]. Плиммер, Р.Х.А .; Хопкинс, Ф.Г. (ред.). Ақуыздардың химиялық құрамы. Биохимия бойынша монографиялар. I бөлім. Талдау (2-ші басылым). Лондон: Longmans, Green and Co. б. 82. Алынған 18 қаңтар, 2010.
- ^ Браконно, Анри (1820). «Sur la conversion des matières animales en nouvelles par par moy moyen de l'acide sulfurique» [Күкірт қышқылы арқылы жануарлардың материалдарын жаңа заттарға айналдыру туралы]. Annales de Chimie et de Physique. 2 серия (француз тілінде). 13: 113–125. ; бетті қараңыз 114.
- ^ МакКензи, Колин (1822). Химиядағы мың тәжірибе: табиғи құбылыстар суреттерімен; Пайдалы өнерді сәтті өсіру барысында қазіргі кездегі өндірістік және химиялық процестерге практикалық бақылаулар…. Сэр Р. Филлипс және Компания. б.557.
- ^ Буссинголь (1838). «Braconnot нитро-сахарик пен гельатиндік композиция» [Желатин қантының және Браконноттың нитро-глюкарин қышқылының құрамы туралы]. Comptes Rendus (француз тілінде). 7: 493–495.
- ^ Хорсфорд, Э.Н. (1847). «Гликоколол (желатинді қант) және оның кейбір ыдырау өнімдері». Американдық ғылым және өнер журналы. 2 серия. 3: 369–381.
- ^ Ихде, Аарон Дж. (1970). Қазіргі химияның дамуы. Courier Corporation. ISBN 9780486642352.
- ^ Берзелиус, Якоб (1848). Jahres-Bericht über die Fortschritte der Chemie und Mineralogie (Химия мен минералогияның дамуы туралы жылдық есеп). т. 47. Тюбиген, (Германия): Лаупп. б. 654. Б. 654: «Er hat dem Leimzucker als Basis den Namen Гликокол гегебен. … Глицин genannt werden, und diesen Namen werde ich anwenden. « (Ол [яғни, американдық ғалым Эбен Нортон Хорсфорд, содан кейін неміс химигінің студенті Юстус фон Либиг ] «гликоколл» атауын берді Леймцукер [желатин қант], негіз. Бұл атау эвониялық емес, сонымен қатар ол басқа негіздердің аттарымен қақтығысатын кемшіліктерге ие. Ол γλυχυς (тәтті) және χολλα (жануарлардың желімі) қоспасынан тұрады. Бұл органикалық негіз тәтті болатын жалғыз [ол] болғандықтан, оны «глицин» деп қысқаша атауға болады, мен бұл атауды қолданамын.)
- ^ Nye, Mary Jo (1999). Үлкен ғылымға дейін: Қазіргі заманғы химия мен физиканы іздеу, 1800-1940 жж. Гарвард университетінің баспасы. ISBN 9780674063822.
- ^ «глицин». Оксфорд сөздіктері. Алынған 2015-12-06.
- ^ Cahours, A. (1858). «Recherches sur les acides amidés» [Амин қышқылдары туралы зерттеулер]. Comptes Rendus (француз тілінде). 46: 1044–1047.
- ^ Окафор, Ндука (2016-03-09). Қазіргі өндірістік микробиология және биотехнология. CRC Press. ISBN 9781439843239.
- ^ Ингерсол, А.В .; Babcock, S. H. (1932). «Гиппур қышқылы». Органикалық синтез. 12: 40.; Ұжымдық көлем, 2, б. 328
- ^ Уили (2007-12-14). Kirk-Omer тамақ және жем беру технологиясы, 2 томдық жинақ. Джон Вили және ұлдары. ISBN 9780470174487.
- ^ «Глицин конференциясы (прелим)». USITC. Түпнұсқадан мұрағатталған 2012-02-22. Алынған 2014-06-13.CS1 maint: BOT: түпнұсқа-url күйі белгісіз (сілтеме)
- ^ а б c Драуз, Карлхейнц; Грейсон, Ян; Климан, Аксель; Криммер, Ханс-Питер; Люхтенбергер, Вольфганг; Векбекер, Кристоф (2007). «Аминоқышқылдар». Ульманның өндірістік химия энциклопедиясы. Вайнхайм: Вили-ВЧ.
- ^ Харт, Дж. Роджер (2005). «Этилендиаминететраасетикалық қышқыл және онымен байланысты хелат агенттері». Ульманның өндірістік химия энциклопедиясы. Вайнхайм: Вили-ВЧ. дои:10.1002 / 14356007.a10_095.
- ^ Ингерсол, А.В .; Babcock, S. H. (1932). «Гиппур қышқылы». Org. Синт. 12: 40. дои:10.15227 / orgsyn.012.0040.
- ^ Хербст, Р.М .; Шемин, Д. (1939). «Ацетилгликин». Org. Синт. 19: 4. дои:10.15227 / orgsyn.019.0004.
- ^ Мелендес-Хевия, Е; Де Паз-Люго, П; Корниш-Боуден, А; Карденас, Л.Л (желтоқсан 2009). «Метаболизмдегі әлсіз байланыс: глицин биосинтезінің метаболизм қабілеті коллаген синтезіне деген қажеттілікті қанағаттандырмайды». Биоғылымдар журналы. 34 (6): 853–72. дои:10.1007 / s12038-009-0100-9. PMID 20093739. S2CID 2786988.
- ^ а б c г. e f ж Нельсон, Дэвид Л .; Кокс, Майкл М. (2005). Биохимияның принциптері (4-ші басылым). Нью-Йорк: В. Х. Фриман. 127, 675–77, 844, 854 беттер. ISBN 0-7167-4339-6.
- ^ а б Хан RG (1993). «Глициннің дозаға тәуелді жартылай шығарылу кезеңі». Урологиялық зерттеулер. 21 (4): 289–291. дои:10.1007 / BF00307714. PMID 8212419. S2CID 25138444.
- ^ ACS Chem Biol. 2010 ж. 20 тамыз; 5 (8): 787-795.doi: 10.1021 / cb100096f
- ^ Spak, Paul (2011). «Балық сүйектерінің химиясы және ультрақұрылымы: тапономия мен тұрақты изотопты талдаудың салдары». Археологиялық ғылымдар журналы. 38 (12): 3358–3372. дои:10.1016 / j.jas.2011.07.022.
- ^ «NMDA рецепторларындағы соңғы даму». Қытай медициналық журналы. 2000.
- ^ «Глицинге арналған қауіпсіздік (MSDS) деректері». Физикалық және теориялық химия зертханасы Оксфорд университеті. 2005. мұрағатталған түпнұсқа 2007-10-20. Алынған 2006-11-01.
- ^ «Жапония мен Кореядан глицин» (PDF). АҚШ Халықаралық сауда комиссиясы. Қаңтар 2008 ж. Алынған 2014-06-13.
- ^ Касари, Б.М .; Махмудхани, А. Х .; Лангер, В. (2004). «Қайта анықтау cis-Аквабис (глицинато-κ)2N, O) мыс (II) «. Acta Crystallogr. E. 60 (12): m1949 – m1951. дои:10.1107 / S1600536804030041.
- ^ Штал, Шеннон С .; Альстер, Пол Л. (2016-07-13). Сұйық фазалы аэробты тотығу катализі: өндірістік қолдану және академиялық перспективалар. Джон Вили және ұлдары. ISBN 9783527690152.
- ^ Квенволден, Кит А .; Заңсыз Джеймс; Перинг, Кэтрин; Петерсон, Этта; Флорес, Хосе; Поннамперума, Кирилл; Каплан, Исаак Р .; Мур, Карлтон (1970). «Жерден тыс амин қышқылдары мен көмірсутектердің Мурчисон метеоритіндегі дәлелдері». Табиғат. 228 (5275): 923–926. Бибкод:1970 ж.228..923K. дои:10.1038 / 228923a0. PMID 5482102. S2CID 4147981.
- ^ «Құйрықты жұлдыздан табылған тіршілік материалы - Thomson Reuters 2009». Reuters. 2009 жылғы 18 тамыз. Алынған 2009-08-18.
- ^ Еуропалық ғарыш агенттігі (2016 ж. 27 мамыр). «Розеттаның кометасында өмірге арналған ингредиенттер бар». Алынған 2016-06-05.
- ^ Снайдер Л.Е., Ловас Ф.Ж., Холлис Дж.М. және т.б. (2005). «Жұлдызаралық глицинді тексеруге қатаң әрекет». Astrophys J. 619 (2): 914–930. arXiv:astro-ph / 0410335. Бибкод:2005ApJ ... 619..914S. дои:10.1086/426677. S2CID 16286204.
- ^ Қызметкерлер құрамы. «Органикалық молекула, амин қышқылына ұқсас, Стрелец жұлдызында табылған 27 наурыз 2008 ж. - Science Daily». Алынған 2008-09-16.
- ^ Трифонов, Е.Н (желтоқсан 2000). «Аминқышқылдарының уақытша тәртібі және триплет кодының эволюциясы». Джин. 261 (1): 139–151. дои:10.1016 / S0378-1119 (00) 00476-5.
- ^ Хиггс, Пол Дж.; Пудриц, Ральф Е. (маусым 2009). «Пребиотикалық амин қышқылын синтездеудің термодинамикалық негізі және алғашқы генетикалық кодтың табиғаты». Астробиология. 9 (5): 483–490. дои:10.1089 / ast.2008.0280. ISSN 1531-1074.
- ^ Халиотис, Анаргирос; Властаридис, Панайотис; Моссиалос, Димитрис; Ибба, Майкл; Беккер, Гюберт Д .; Статопулос, Константинос; Амуциас, Григориос Д. (2017-02-17). «Аминоацил-тРНҚ синтетазаларының күрделі эволюциялық тарихы». Нуклеин қышқылдарын зерттеу. 45 (3): 1059–1068. дои:10.1093 / nar / gkw1182. ISSN 0305-1048. PMC 5388404. PMID 28180287.
- ^ а б Нтаунтоуми, Хриса; Властаридис, Панайотис; Моссиалос, Димитрис; Статопулос, Константинос; Илиопулос, Иоаннис; Промпоналар, Василиос; Оливер, Стивен Дж; Амуциас, Григорис Д (2019-11-04). «Прокариоттардың ақуыздарындағы күрделілігі төмен аймақтар маңызды функционалды рөлдерді орындайды және жоғары деңгейде сақталады». Нуклеин қышқылдарын зерттеу. 47 (19): 9998–10009. дои:10.1093 / nar / gkz730. ISSN 0305-1048. PMC 6821194. PMID 31504783.
- ^ «Стандартты анықтама үшін ұлттық қоректік заттар базасы». АҚШ ауылшаруашылық департаменті. Архивтелген түпнұсқа 2015-03-03. Алынған 2009-09-07. Журналға сілтеме жасау қажет
| журнал =(Көмектесіңдер)
Әрі қарай оқу
- Kuan YJ, Charnley SB, Huang HC және т.б. (2003). «Жұлдызаралық глицин». Astrophys J. 593 (2): 848–867. Бибкод:2003ApJ ... 593..848K. дои:10.1086/375637.
- Новак, Рейчел. «Амин қышқылы терең кеңістіктен табылды - 2002 ж. 18 шілде - Жаңа ғалым". Алынған 2007-07-01.
Сыртқы сілтемелер
- Глицин MS спектрі
- Глицин PDRHealth.com сайтында
- Глицинді бөлшектеу жүйесі
- Глицин терапиясы - шизофренияны емдеудің жаңа бағыты?
- «Стрелец жұлдызында кездесетін аминқышқылы тәрізді органикалық молекула». ScienceDaily. 27 наурыз 2008 ж.
- Цай, Гочуань Э. (1 желтоқсан 2008). «Антипсихотикалық препараттардың жаңа класы: NMDA рецепторларының көмегімен нейротрансмиссияны күшейту». Психиатриялық Times. 25 (14).
- ChemSub Online (глицин).
- NASA ғалымдары NASA-ның Stardust ғарыш кемесі қайтарған Wild 2 кометасының үлгілерінен тіршіліктің негізін қалайтын глицин тапты.