Эндометриялық қатерлі ісік - Endometrial cancer - Wikipedia
| Эндометриялық қатерлі ісік | |
|---|---|
| Басқа атаулар | Жатырдың қатерлі ісігі |
 | |
| Эндометриялық қатерлі ісіктің орналасуы және дамуы. | |
| Мамандық | Онкология, гинекология |
| Белгілері | Қынаптан қан кету, зәр шығару кезінде ауырсыну немесе жыныстық қатынас, жамбастың ауыруы[1] |
| Әдеттегі басталу | Кейін менопауза[2] |
| Тәуекел факторлары | Семіздік, шамадан тыс эстроген экспозиция, Жоғарғы қан қысымы, қант диабеті, отбасылық тарих[1][3] |
| Диагностикалық әдіс | Эндометриялық биопсия[1] |
| Емдеу | Іштің гистерэктомиясы, сәулелік терапия, химиотерапия, гормондық терапия[4] |
| Болжам | Бес жылдық өмір сүру деңгейі ~ 80% (АҚШ)[5] |
| Жиілік | 3,8 млн (жалпы 2015 ж. Зардап шеккен)[6] |
| Өлімдер | 89,900 (2015)[7] |
Эндометриялық қатерлі ісік Бұл қатерлі ісік туындаған эндометрия ( төсеу туралы жатыр немесе жатыр).[1] Бұл қалыптан тыс өсудің нәтижесі жасушалар басып кіру немесе дененің басқа бөліктеріне таралу мүмкіндігі бар.[8] Бірінші белгі жиі кездеседі қынаптан қан кету байланысты емес етеккір кезеңі.[1] Басқа белгілерге жатады зәр шығару кезінде ауырсыну, жыныстық қатынас кезінде ауырсыну, немесе жамбастың ауыруы.[1] Эндометриялық қатерлі ісік көбінесе кейін пайда болады менопауза.[2]
Істердің шамамен 40% байланысты семіздік.[3] Эндометрия қатерлі ісігі де шамадан тыс асқынумен байланысты эстроген экспозиция, Жоғарғы қан қысымы және қант диабеті.[1] Тек эстрогенді қабылдау эндометриялық қатерлі ісік қаупін арттырады, ал эстрогенді де, а прогестоген көпшілігінде сияқты үйлесімде босануды бақылауға арналған таблеткалар, тәуекелді азайтады.[1][3] Екі-бес пайыз аралығында ата-анадан мұраға қалған гендерге қатысты.[3] Эндометрия қатерлі ісігі кейде «еркін» деп аталадыжатырдың қатерлі ісігі сияқты, жатыр қатерлі ісігінің басқа түрлерінен ерекше болғанымен жатыр мойны обыры, жатыр саркомасы, және трофобластикалық ауру.[9] Ең жиі түрі эндометрия қатерлі ісігі эндометриоидты болып табылады карцинома, бұл жағдайлардың 80% -дан астамын құрайды.[3] Эндометрия қатерлі ісігі, әдетте, диагноз қойылады эндометрия биопсиясы немесе белгілі процедура кезінде сынамалар алу арқылы кеңейту және кюретаж.[1] A пап жағындысы эндометрия қатерлі ісігін көрсету үшін әдетте жеткіліксіз.[4] Қалыпты тәуекелге ұшырағандарға үнемі скрининг жүргізу қажет емес.[10]
Эндометрия қатерлі ісігін емдеудің жетекші нұсқасы болып табылады іш қуысының гистерэктомиясы (толық жою хирургия алып тастаумен бірге) Фаллопиялық түтіктер және аналық без екі жақты деп аталатын екі жақты сальпинго-оофорэктомия.[4] Жетілдірілген жағдайларда, сәулелік терапия, химиотерапия немесе гормондық терапия ұсынылуы мүмкін.[4] Егер ауру ерте анықталса кезең, нәтиже қолайлы,[4] және жалпы бес жылдық өмір сүру деңгейі АҚШ-та 80% -дан жоғары.[5]
2012 жылы эндометриялық қатерлі ісіктер 320 000 әйелде жаңадан пайда болып, 76 000 адамның өліміне әкелді.[3] Бұл оны әйелдерге ғана қатысты болатын қатерлі ісіктердегі өлім-жітімнің үшінші себебі болып табылады аналық без және жатыр мойны обыры.[3] Бұл дамыған елдерде жиі кездеседі[3] және ең таралған қатерлі ісік әйелдердің репродуктивті трактісі дамыған елдерде.[4] 1980 - 2010 жылдар аралығында бірқатар елдерде эндометрия қатерлі ісігінің деңгейі жоғарылаған.[3] Бұл егде жастағы адамдар санының көбеюіне және семіздік деңгейінің артуына байланысты деп санайды.[11]
Белгілері мен белгілері
Қынаптан қан кету немесе кейінгі әйелдерде байқау менопауза эндометрия обырының 90% -ында кездеседі.[2][13][14] Қан кету әсіресе жиі кездеседі аденокарцинома, барлық жағдайлардың үштен екісінде кездеседі.[2][10] Қалыптан тыс етеккір циклдары немесе менопаузаға дейін әйелдердің қан кетуінің өте ұзақ, ауыр немесе жиі болатын эпизодтары эндометрия обырының белгісі болуы мүмкін.[10]
Қан кетуден басқа белгілер жиі кездеспейді. Басқа белгілерге жіңішке ақ немесе ашық түсті жатады вагинальды разряд постменопаузды әйелдерде. Неғұрлым дамыған ауру а-да анықталатын айқын белгілерді немесе белгілерді көрсетеді физикалық тексеру. Жатырдың ұлғаюы немесе қатерлі ісіктің таралуы мүмкін, іштің төменгі бөлігінде ауырсыну немесе жамбас сүйектері ауырады.[10] Ауырсыну жыныстық қатынас немесе ауыр немесе қиын зәр шығару эндометрия қатерлі ісігінің сирек кездесетін белгілері.[9] Жатыр сонымен бірге толтырылуы мүмкін ірің (пиометрия ).[15] Осындай сирек кездесетін белгілері бар әйелдердің (қынаптан бөліну, жамбастың ауыруы және ірің) 10-15% -ы қатерлі ісікке шалдыққан.[16]
Тәуекел факторлары
Эндометрия қатерлі ісігінің факторларына жатады семіздік, қант диабеті, сүт безі қатерлі ісігі, қолдану тамоксифен, ешқашан бала көрмеген, кеш климакс, жоғары деңгей эстроген және жасы ұлғайып келеді.[15][16] Иммиграциялық зерттеулер (миграциялық зерттеулер), қатерлі ісік деңгейі әр түрлі елдер арасында қозғалатын популяциялардағы қатерлі ісік қаупінің өзгеруін зерттейді, эндометрия обырының кейбір экологиялық компоненттері бар екенін көрсетеді.[17] Бұл экологиялық тәуекел факторлары жақсы сипатталмаған.[18]
Гормондар
Эндометрия қатерлі ісігінің қауіпті факторларының көпшілігінде эстрогендердің жоғары деңгейі бар. Шамамен 40% жағдай семіздікпен байланысты деп есептеледі.[3] Семіздік кезінде артық май тіні түрлендіруді жоғарылатады андростендион ішіне эстрон, эстроген. Қандағы эстрон деңгейінің жоғарылауы себеп болады Аздау немесе овуляция жоқ эндометрияны үнемі жоғары деңгейдегі эстрогендерге ұшыратады.[11][19] Семіздік сонымен қатар қандағы эстрогеннің аз мөлшерде кетуіне әкеледі.[19] Поликистозды аналық без синдромы (PCOS), сонымен қатар овуляцияны тұрақты емес немесе жоқ етеді, семіздік сияқты себептер бойынша эндометрия қатерлі ісігінің жоғарылауымен байланысты.[17] Нақтырақ айтқанда, семіздік, II типті қант диабеті және инсулинге төзімділік I типті эндометрия қатерлі ісігінің қауіпті факторлары болып табылады.[20] Семіздік эндометрия рагының даму қаупін 300-400% арттырады.[21]
Эстрогенді алмастыру терапиясы менопауза кезінде теңдестірілмеген (немесе «қарсы») прогестин тағы бір қауіп факторы болып табылады. Эстрогенді терапияның жоғарырақ дозалары немесе ұзағырақ кезеңдері эндометрия обырының жоғары қаупіне ие.[19] Төмен салмақтағы әйелдерге қарсылықсыз эстрогеннің қаупі жоғары.[3] Ұрықтанудың ұзағырақ кезеңі - ерте кезден бастап бірінші етеккір немесе кеш менопауза - бұл сондай-ақ қауіпті фактор.[22] Қарсыласпаған эстроген терапияның салмағы мен ұзақтығына байланысты адамның эндометрия рагы қаупін 2-10 есе арттырады.[3] Жылы транс ерлер кім алады тестостерон және гистерэктомия жасамаған, тестостеронның андростендион арқылы эстрогенге айналуы эндометрия қатерлі ісігінің жоғарылауына әкелуі мүмкін.[23]
Генетика

Генетикалық бұзылулар сонымен қатар эндометрия қатерлі ісігін тудыруы мүмкін. Тұтастай алғанда, тұқым қуалайтын себептер эндометриялық қатерлі ісіктердің 2–10% -ын құрайды.[3][24] Линч синдромы, an аутосомды доминант негізінен тудыратын генетикалық бұзылыс тік ішек рагы, сонымен қатар эндометрия обырын тудырады, әсіресе менопаузаға дейін. Линч синдромы бар әйелдердің эндометрия рагының даму қаупі 40-60% құрайды, бұл олардың колоректалды (ішек) немесе аналық без рагының даму қаупінен жоғары.[17] Аналық без және эндометрия қатерлі ісігі адамдардың 20% -ында бір мезгілде дамиды. Эндометриялық қатерлі ісік әрдайым тоқ ішектің қатерлі ісігіне дейін дамиды, орта есеппен 11 жыл бұрын.[18] Канцерогенез Линч синдромында мутация пайда болады MLH1 немесе MLH2: процесіне қатысатын гендер сәйкессіздікті жөндеу, бұл жасушаға ДНҚ-дағы қателерді түзетуге мүмкіндік береді.[17] Линч синдромында мутацияға ұшыраған басқа гендерге жатады MSH2, MSH6, және PMS2, олар сәйкес келмейтін жөндеу гендері болып табылады. Линч синдромы бар әйелдер эндометриялық қатерлі ісіктің 2-3% құрайды; кейбір ақпарат көздері мұны 5% -ке дейін жеткізеді.[18][21] Гендік мутацияға байланысты, Линч синдромы бар әйелдер эндометрия қатерлі ісігінің әр түрлі қаупіне ие. MLH1 мутациясымен тәуекел 54% құрайды; MSH2-мен, 21%; және MSH6-мен 16%.[25]
Отбасылық эндометрия қатерлі ісігі бар әйелдер қаупі жоғары.[9] Әйелдер қатерлі ісіктерімен жиі кездесетін екі ген, BRCA1 және BRCA2, эндометрия қатерлі ісігін тудырмаңыз. Бұл гендермен анық байланыс бар, бірақ бұл эндокриндік қатерлі ісік ауруын тудыруы мүмкін тамоксифен препаратын сүт безі мен аналық без қатерлі ісіктерінде қолдануға байланысты.[17] Тұқым қуалайтын генетикалық жағдай Коуден синдромы сонымен қатар эндометрия қатерлі ісігін тудыруы мүмкін. Мұндай бұзылысы бар әйелдерде эндометрия қатерлі ісігінің даму қаупі 5-10% құрайды,[3] зардап шекпеген әйелдер үшін 2-3% қаупімен салыстырғанда.[18]
Жалпы генетикалық вариация сонымен қатар эндометрия қатерлі ісігінің кең ауқымда әсер ететіндігі анықталды жалпы геномды ассоциацияны зерттеу.[26][27] Он алты геномдық аймақ эндометрия қатерлі ісігімен байланысты болды және жалпы нұсқалары отбасылық салыстырмалы қауіптің 7% -на дейін түсіндіреді.[27]
Денсаулықтың басқа мәселелері
Қатерлі ісіктің басқа түрлерін емдеудің кейбір әдістері эндометрия қатерлі ісігінің өмірлік қаупін арттырады, бұл базалық деңгей 2-3% құрайды.[18] Тамоксифен, емдеуге арналған препарат эстроген-оң сүт безі қатерлі ісіктері, қолданушылардың шамамен 0,1% -ында, әсіресе егде жастағы әйелдерде эндометрия қатерлі ісігімен байланысты болды, бірақ тамоксифеннен аман қалудың артықшылығы эндометрия қатерінен жоғары.[28] Тамоксифеннің бір-екі жылдық курсы эндометрия рагының даму қаупін шамамен екі есеге арттырады, ал бес жылдық терапия бұл қауіпті төрт есе арттырады.[22] Ралоксифен, ұқсас препарат эндометрия қатерлі ісігінің қаупін тудырмады.[29] Бұрын болған аналық без қатерлі ісігі эндометрия қатерлі ісігінің қауіпті факторы болып табылады,[30] бұған дейін жамбасқа сәулелік терапия жүргізгендей. Нақтырақ айтқанда, аналық без гранулеза жасушаларының ісіктері және comcom эндометриялық қатерлі ісікпен байланысты ісіктер.
Төмен иммундық функция эндометрия қатерлі ісігіне де қатысты болды.[15] Жоғарғы қан қысымы сонымен қатар тәуекел факторы болып табылады,[21] бірақ бұл оның семіздікпен байланысы болуы мүмкін.[25] Отыру үнемі ұзақ уақыт бойы эндометрия қатерлі ісігінен болатын өлімнің жоғарылауымен байланысты. Тәуекел тұрақты жаттығулармен жойылмайды, дегенмен ол төмендетілген.[31]
Қорғаныс факторлары
Темекі шегу және прогестинді қолдану эндометрия обырынан қорғайды. Темекі шегу эстрогендердің метаболизмін өзгерту және салмақ жоғалтуға және ерте менопаузаға ықпал ету арқылы қорғауды қамтамасыз етеді. Бұл қорғаныс әсері темекі шегуден бас тартқаннан кейін ұзақ уақыт сақталады. Прогестин құрамында болады аралас ішілетін контрацепция таблетка және гормоналды жатырішілік құрал (Спираль).[17][32] Біріктірілген пероральді контрацептивтер қауіпті төмендететін уақытты азайтады: төрт жылдан кейін 56%, сегіз жылдан кейін 67%, он екі жылдан кейін 72%. Қауіптің төмендеуі контрацепцияны қолдануды тоқтатқаннан кейін кем дегенде он бес жыл бойы жалғасады.[29] Семіздікке ұшыраған әйелдерді қорғау үшін прогестиннің жоғары дозалары қажет болуы мүмкін.[32] Бес баладан көп болу (үлкен көпшілік) - бұл қорғаныс факторы,[15] және кем дегенде бір баланың болуы қауіпті 35% төмендетеді. 18 айдан астам емізу қауіпті 23% төмендетеді. Дене белсенділігінің жоғарылауы адамның тәуекелін 38-46% төмендетеді. Тұтыну туралы алдын-ала дәлелдемелер бар соя қорғаныс.[29]
Патофизиология
 Жатыр қабырғасы ұлғайған және қалыпты эндометрия көрінетін әйелдердің репродуктивті жолын көрсететін диаграмма | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Эндометриялық қатерлі ісік қалыпты эндометрияда қателіктер болған кезде пайда болады жасушалардың өсуі. Әдетте, жасушалар қартайғанда немесе зақымданғанда, олар өлу және олардың орнына жаңа жасушалар келеді. Қатерлі ісік жаңа жасушалар қажетсіз пайда болған кезде басталады, ал ескі немесе зақымдалған жасушалар қажет болған жағдайда өлмейді. Қосымша жасушалардың өсуі көбінесе өсу немесе ісік деп аталатын тіндердің массасын құрайды. Бұл аномальды рак клеткаларында көп генетикалық ауытқулар олардың шамадан тыс өсуіне себеп болады.[9]
Эндометриялы қатерлі ісіктердің 10-20% -ында, көбінесе 3 дәрежесі (ең жоғары) гистологиялық дәреже ), мутациялар а ісік супрессоры ген, әдетте p53 немесе PTEN. 20% -да эндометриялық гиперплазиялар және 50% эндометриоидты қатерлі ісіктер, PTEN а функцияны жоғалту мутациясы немесе а нөлдік мутация, оны аз тиімді немесе мүлдем тиімсіз ету.[34] PTEN функциясының жоғалуы жасушалардың өсуіне себеп болатын PI3k / Akt / mTOR жолының реттелуіне әкеледі.[21] Р53 жолы басылуы немесе эндометрия қатерлі ісігі кезінде өте белсенді болуы мүмкін. Р53 мутантты нұсқасы шамадан тыс әсер етсе, қатерлі ісік әсіресе агрессивті болады.[34] P53 мутациясы және хромосомалардың тұрақсыздығы аналық және фаллопиялық карциномаларға ұқсайтын серозды карциномалармен байланысты. Серозды карциномалар пайда болады деп ойлайды эндометрия ішілік эпителиальды карцинома.[21]
PTEN және б27 функционалды мутациялардың жоғалуы жақсы болжаммен байланысты, әсіресе семіз әйелдерде. The Her2 / neu онкоген, бұл нашар болжамды көрсетеді, эндометриоидты және сероздық карциномалардың 20% -ында көрінеді. CTNNB1 (бета-катенин; а транскрипция ген) мутациялар эндометриялық қатерлі ісіктердің 14-44% -ында кездеседі және жақсы болжамды көрсете алады, бірақ мәліметтер түсініксіз.[34] Бета-катенин мутациясы әдетте эндометриялық қатерлі ісіктерде кездеседі қабыршақ жасушалар.[21] FGFR2 мутациялар эндометриялық қатерлі ісіктердің шамамен 10% -ында кездеседі және олардың болжамдық маңызы түсініксіз.[34] SPOP - эндометрия қатерлі ісігінің кейбір жағдайларында мутацияға ұшыраған тағы бір ісік супрессоры гені: эндометриялы клеткалардың 9% -ы және сероздық эндометриялық карциномалардың 8% -ында осы генде мутация бар.[35]
І және ІІ типті қатерлі ісік аурулары (төменде түсіндірілген) әртүрлі мутацияларға ұшырайды. ARID1A, ол жиі а нүктелік мутация І типті эндометрия қатерлі ісігінде эндометрияның мөлдір жасушалы карциномаларының 26% -ында және сероздық карциномалардың 18% -ында мутацияға ұшыраған. Эпигенетикалық тыныштық және эндометриялық қатерлі ісік кезінде бірнеше гендердің нүктелік мутациясы жиі кездеседі.[3][33] Ісік супрессоры гендерінің мутациясы эндометрия қатерлі ісігінің II типінде жиі кездеседі.[3] PIK3CA I типтегі және II типті қатерлі ісіктерде әдетте мутацияға ұшырайды.[33] Линч синдромымен байланысты эндометрия қатерлі ісігі бар әйелдерде, микроспутниктің тұрақсыздығы кең таралған.[21]
Әзірлеу эндометрия гиперплазиясы (эндометрия жасушаларының шамадан тыс өсуі) - бұл маңызды қауіп факторы, себебі гиперплазиялар аденокарциномаға айналуы мүмкін және көбінесе дамиды, бірақ қатерлі ісік гиперплазиясыз дамиды.[19] Он жыл ішінде эндометриялы атипті гиперплазиялардың 8-30% -ы қатерлі ісікке айналады, ал типтік емес гиперплазиялардың 1-3% -ы жасайды.[36] Атипиялық гиперплазия - бұл көрінетін ауытқулар ядролар. Қатерлі ісік алдындағы эндометрия гиперплазиясы деп те аталады эндометрия ішілік эпителиальді неоплазия.[37] Мутациялар KRAS ген эндометрия гиперплазиясын тудыруы мүмкін, сондықтан эндометрияның I типті қатерлі ісігі.[34] Эндометрия гиперплазиясы әдетте 40 жастан кейін пайда болады.[9] Эндометриялық безді дисплазия р53 шамадан тыс экспрессиясында пайда болады және серозды карциномаға айналады.[15]
Диагноз
Эндометрия қатерлі ісігінің диагностикасы алдымен физикалық тексеру, эндометрия биопсиясы немесе кеңейту және кюретаж (эндометрия тінін жою; D&C). Содан кейін бұл мата қатерлі ісік сипаттамалары үшін гистологиялық зерттеледі. Егер қатерлі ісік табылса, онда медициналық суреттің көмегімен қатерлі ісіктің таралғанын немесе тіндерге еніп кеткендігін анықтауға болады.
Сараптама
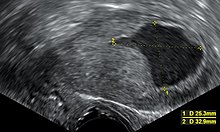

Асимптоматикалық адамдарды жоспарлы скринингтен өткізу көрсетілмеген, себебі ауру ерте, симптоматикалық сатысында өте жақсы емделеді. Керісінше, әйелдер, әсіресе менопауза кезеңіндегі әйелдер эндометрия қатерлі ісігінің белгілері мен қауіп факторларын білуі керек. A жатыр мойны скринингі сынақ, мысалы Pap smear, эндометриялық қатерлі ісіктің пайдалы диагностикалық құралы емес, себебі жағынды 50% қалыпты болады.[10] Пап жағындысы жатыр мойнына таралған ауруды анықтай алады.[9] Нәтижелері жамбас зерттеуі жиі қалыпты, әсіресе аурудың алғашқы кезеңінде. Жатырдың немесе оны қоршайтын құрылымдардың мөлшерінің, формасының немесе консистенциясының өзгеруі ауру асқынған кезде болуы мүмкін.[10] Жатыр мойнының стенозы, жатыр мойнының саңылауының тарылуы, жатырда жиналған ірің немесе қан табылған кезде эндометрия обырының белгісі болып табылады (пиометра немесе гематометрия ).[13]
Әйелдер Линч синдромы 35 жасында жыл сайынғы биопсиялық скринингтен өтуі керек. Линч синдромымен ауыратын кейбір әйелдер эндометрия мен аналық без қатерлі ісігінің қаупін едәуір азайту үшін профилактикалық гистерэктомия және сальпинго-оофорэктомия жасауды таңдайды.[10]
Трансвагиналды ультрадыбыстық постменопаузды қан кетуімен ауыратын әйелдердің эндометрия қалыңдығын зерттеу үшін Америка Құрама Штаттарында эндометрия обырын диагностикалауға көбірек қолданылады.[38] Ұлыбританияда екеуі де эндометрия биопсиясы және трансвагинальды ультрадыбыспен бірге қолданылатын эндометриялық қатерлі ісіктерді диагностикалаудың стандарттары болып табылады.[15] Трансвагиналды ультрадыбыста көрінетін тіннің біртектілігі қалыңдығының қатерлі ісік екенін анықтауға көмектеседі. Эндометрияның қатерлі ісігі жағдайында ультрадыбыстық зерттеулердің нәтижелері жалғыз емес, сондықтан скринингтің басқа әдісін (мысалы, эндометрия биопсиясы) бірге қолдану қажет. Басқа бейнелеу зерттеулерінің қолданылуы шектеулі. Томографиялық томография физикалық емтиханда дамыған немесе жоғары тәуекелді подтипі бар ісіктерді операцияға дейін бейнелеу үшін қолданылады (жоғары тәуекел жағдайында) метастаз ).[39] Олар сондай-ақ экстрапельвистикалық ауруды зерттеу үшін қолданыла алады.[15] Ан МРТ қатерлі ісіктің жатыр мойнына таралғанын немесе бұл эндоцервикальді аденокарцинома екенін анықтауда біраз қолданылуы мүмкін.[39] МРТ жақын орналасқан лимфа түйіндерін зерттеу үшін де пайдалы.[15]
Гистологиялық зерттеу үшін тіндік үлгіні алу үшін кеңейту және кюретаж немесе эндометрия биопсиясы қолданылады. Эндометриялық биопсия - бұл аз инвазивті нұсқа, бірақ ол әрдайым нәтиже бермеуі мүмкін. Гистероскопия эндометрияның жалпы анатомиясын ғана көрсетеді, ол көбінесе қатерлі ісік туралы белгі бермейді, сондықтан биопсиямен бірге болмаса, қолданылмайды.[39] Гистероскопияны қатерлі ісік диагнозын растау үшін қолдануға болады. Жаңа дәлелдемелер D&C эндометрия биопсиясына қарағанда жалған теріс жылдамдықтың жоғары екендігін көрсетеді.[21]
Емдеу басталғанға дейін бірнеше басқа зерттеулер ұсынылады. Оларға кеуде қуысының рентгенографиясы, бауыр функциясының сынақтары, бүйрек функциясының сынақтары,[21] және деңгейлеріне арналған тест CA-125, а ісік маркері эндометриялық қатерлі ісік кезінде жоғарылауы мүмкін.[9]
Жіктелуі
Эндометриялық қатерлі ісіктер эпителий жасушаларынан алынған ісіктер болуы мүмкін (карциномалар), аралас эпителий және мезенхимальды ісіктер (карциносаркома) немесе мезенхималық ісіктер.[40]

Эндометриялық карциномалардың дәстүрлі классификациясы клиникалық және эндокриндік ерекшеліктерге (I тип және II тип) немесе гистопатологиялық сипаттамаларға (эндометриоидты, серозды және клеткалық) негізделген. Кейбір ісіктерді жіктеу қиын және олардың ерекшеліктері бірнеше санатпен қабаттасады. Жоғары деңгейлі эндометриоидты ісіктер, атап айтқанда, I типке де, II типке де ие.[40]
Карцинома
Эндометриялық қатерлі ісіктердің басым көпшілігі карциномалар (әдетте аденокарциномалар), яғни олар бір қабатынан пайда болады эпителий эндометрияны қаптап, эндометрия бездерін құрайтын жасушалар. Мұнда көптеген бар микроскопиялық эндометриялы карциноманың кіші түрлері, бірақ олар клиникалық ерекшеліктері мен патогенезіне негізделген I және II типті екі категорияға бөлінген. Екі кіші тип генетикалық жағынан ерекшеленеді.[10]
I типті эндометрия карциномалары көбінесе менопауза басталғанға дейін және айналасында пайда болады. Америка Құрама Штаттарында олар жиі кездеседі ақ әйелдер, әсіресе эндометрия гиперплазиясы тарихы барлар. І типті эндометриялық қатерлі ісіктер көбінесе төменгі дәрежелі, жатырдың төменгі қабырғаларына инвазивті (миометрия ), эстрогенге тәуелді және емдеудің нәтижесі жақсы.[10] І типті карциномалар эндометрия обырының 75-90% құрайды.[15][42]
Эндометрияның II типті карциномалары әдетте егде жастағы, менопаузадан кейінгі адамдарда кездеседі, Америка Құрама Штаттарында жиі кездеседі қара әйелдер, және эстрогеннің жоғарылауымен немесе эндометрия гиперплазиясының тарихымен байланысты емес. II типті эндометриялық қатерлі ісіктер көбінесе жоғары дәрежелі, жатырдың төменгі қабырғасына (миометрияға) терең енуімен, серозды немесе таза ұяшық және кедей болжамды көрсетіңіз. Олар болуы мүмкін эпителий аналық безінің қатерлі ісігі белгілерді бағалау туралы.[10][42] Олар І типті ісіктерге қарағанда кешірек пайда болады және агрессивті, рецидивтің және / немесе метастаздың пайда болу қаупі жоғары.[15]
Эндометриоидты аденокарцинома
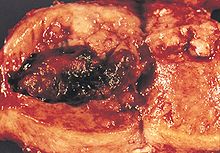

Жылы эндометриоид аденокарцинома, қатерлі ісік жасушалары қалыпты эндометрияны еске түсіретін қалыпта өседі, көптеген жаңа бездер пайда болған бағаналы эпителий кейбірімен қалыптан тыс ядролар. Төмен дәрежелі эндометриоидты аденокарциномалар жасушалары жақсы дифференциалданған, миометрияға енбеген және эндометрия гиперплазиясымен қатар көрінеді. Ісік бездері бір-біріне өте жақын түзіледі стромальды қалыпты жағдайда оларды бөлетін тін. Жоғары дәрежелі эндометриоидты аденокарциномалардың дифференциалданған жасушалары аз, ісік жасушаларының қатты парақтары бездерге бөлінбейді және олармен байланысқан атрофияланған эндометрия. Эндометриоидты аденокарциноманың ұқсас болжамдары бар бірнеше кіші типтері бар, оның ішінде виллогландулярлы, секреторлы және кірпікшелі варианттар бар. Сипатталатын кіші түрі де бар қабыршақ саралау. Кейбір эндометриоидты аденокарциномаларда муцинозды карцинома ошақтары болады.[43]
Эндометриоидты аденокарциномамен жиі байланысты генетикалық мутациялар ісік супрессоры PTEN гендерінде болады; PIK3CA, а киназа; КРАС, а GTPase функциялары сигнал беру; және CTNNB1, адгезия мен жасушалық сигнализацияға қатысады. CTNNB1 (бета-катенин) гені көбінесе эндометриоидты аденокарциноманың жазық кіші түрінде мутацияға ұшырайды.[44]
Серозды карцинома
Сероздық карцинома - эндометрияның II типті ісігі, диагноз қойылған эндометрия рагының 5-10% құрайды және менопаузадан кейінгі эндометриямен атрофияланған әйелдерде және қара әйелдерде жиі кездеседі. Серозды эндометрия карциномасы агрессивті болып табылады және миометрияға жиі еніп, перитонеум ішінде метастаз жасайды (ретінде көрінеді) майлы пирожныйлар ) немесе лимфа жүйесі. Гистологиялық тұрғыдан ол көптеген атиптік ядролармен бірге пайда болады, папиллярлы құрылымдар, және, эндометриоидты аденокарциномалардан айырмашылығы, бағаналы жасушалардың орнына дөңгелектелген жасушалар. Эндометриялық серозды карциномалардың шамамен 30% -ы бар псаммома денелері.[19][42] Серозды карциномалар көптеген эндометриялық қатерлі ісіктерге қарағанда әр түрлі таралады; олар миометрияға енбей жатырдан тыс таралуы мүмкін.[19]
Сероздық карциномада байқалатын генетикалық мутациялар болып табылады хромосомалық тұрақсыздық және мутация TP53, маңызды ісікті басатын ген.[44]
Мөлдір жасушалық карцинома
Мөлдір жасушалы карцинома - бұл эндометриялы ісіктің диагнозы қойылған 5% -дан азды құрайтын II типті эндометрия ісігі. Сероздық жасушалы карцинома сияқты, ол әдетте агрессивті және нашар болжам жасайды. Гистологиялық тұрғыдан ол бәріне ортақ белгілерімен сипатталады мөлдір жасушалар: аттас айқын цитоплазма қашан H&E боялған және көрінетін, айқын жасушалық мембраналар.[42] Р53 жасушалық сигнал беру жүйесі эндометриялы ашық жасушалы карциномада белсенді емес.[15] Эндометрия қатерлі ісігінің бұл түрі менопаузадан кейінгі әйелдерде жиі кездеседі.[19]
Шырышты карцинома
Шырышты карциномалар - эндометриялық қатерлі ісіктің сирек кездесетін түрі, барлық диагноз қойылған эндометрия обырының 1-2% -нан азын құрайды. Мукинді эндометриялы карциномалар көбінесе I және I дәрежелі болып, оларға жақсы болжам жасайды. Әдетте олардың сипаттамасымен бездерге бөлінген жақсы ажыратылған бағаналы жасушалары бар муцин цитоплазмада. Мукинді карциномалар дифференциалдануы керек жатыр мойны аденокарциномасы.[43]
Аралас немесе сараланбаған карцинома
Аралас карциномаларға I типті де, II типті де жасушалар кіреді, олардың біреуі ісіктің кем дегенде 10% құрайды.[43] Оларға қатерлі ісік жатады аралас Мюллерия ісігі, бұл эндометрия эпителийінен шыққан және болжам нашар.[45]
Дифференциалданбаған эндометрия карциномалары диагноз қойылған эндометрия қатерлі ісіктерінің 1-2% -дан азын құрайды. Олар III дәрежелі ісіктерге қарағанда нашар болжам жасайды. Гистологиялық тұрғыдан алғанда, бұл ісіктерде эпителий жасушаларының парақтары анықталмаған, олар анықталмаған.[43]
Басқа карциномалар
Метастатикалық емес қабыршақты карцинома және өтпелі жасушалық карцинома эндометрияда өте сирек кездеседі. Эндометрияның скамозды жасушалы карциномасы нашар болжамға ие.[43] Медициналық әдебиеттерде 1892 жылы сипатталғаннан бері бұл туралы 100-ден аз рет айтылды. Эндометрияның (PSCCE) алғашқы скамозды жасушалы ісігі диагнозын қою үшін эндометрияда немесе жатыр мойнында басқа алғашқы қатерлі ісік болмауы керек және ол болмауы керек. жатыр мойнының эпителийіне байланысты. Бұл қатерлі ісік сирек кездесетіндіктен, оны қалай емдеу керектігі туралы нұсқаулар да, типтік емдеу де жоқ. Жалпы генетикалық себептер сипатталмаған болып қалады.[46] Эндометрияның өтпелі жасушалық карциномалары одан да сирек кездеседі; 2008 жыл бойынша 16 жағдай тіркелді[жаңарту]. Оның патофизиологиясы мен емдеу әдістері сипатталмаған.[47] Гистологиялық тұрғыдан TCCE эндометриоидты карциномаға ұқсайды және басқа өтпелі жасушалық карциномалардан ерекшеленеді.[48]
Саркома

Эндометриялық карциномалардан айырмашылығы, сирек кездесетін эндометрия стромалы саркомалар безді емес пайда болатын қатерлі ісіктер дәнекер тін эндометрия. Олар әдетте агрессивті емес, егер олар қайталанса, ондаған жылдарға созылуы мүмкін. Өкпеге және жамбасқа немесе перитонеальды қуысқа метастаздар жиі кездеседі.[19] Оларда әдетте эстроген және / немесе прогестерон рецепторлары бар.[49] Төмен дәрежелі эндометриялы стромальды саркоманың болжамы жақсы, 60-90% бес жылдық өмір сүру. Жоғары деңгейлі сараланбаған эндометрия саркомасы (HGUS) болжамның нашарлауы бар, қайталанудың жоғары қарқыны және 25% тірі қалу.[50] HGUS болжамы ісіктің тамырлар мен тамырларға енген-кірмегендігімен белгіленеді. Тамырлы инвазиясыз, бес жылдық өмір 83% құрайды; тамырлы инвазия байқалған кезде ол 17% дейін төмендейді. I кезең ЭСЖ ең жақсы болжамға ие, оның бес жылдық өмір сүруі 98%, он жылдық өмірі 89%. ESS жатырдың қатерлі ісіктерінің 0,2% құрайды.[51]
Метастаз
Эндометриялық қатерлі ісік жиі аналық бездерге және фаллопиялық түтіктерге метастаз береді[30] қатерлі ісік жатырдың жоғарғы бөлігінде, ал рак жатырдың төменгі бөлігінде болған кезде жатыр мойны. Қатерлі ісік әдетте миометрияға және сероза, содан кейін басқа репродуктивті және жамбас құрылымдарына. Қашан лимфа жүйесі қатысады, жамбас және пара-қолқа түйіндері Әдетте олар бірінші рет қатысады, бірақ жатыр мойны обырынан айырмашылығы жоқ. Алыстағы метастаздар қанмен таралады және өкпеде, сонымен қатар бауырда, мида және сүйекте жиі кездеседі.[52] Эндометрия қатерлі ісігі кез-келген гинекологиялық қатерлі ісікке қарағанда өкпенің 20-25% метастаз жасайды.[53]
Гистопатология


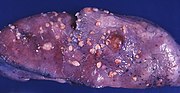
Жақсы дифференциалданған клеткалары бар қатерлі ісіктерден (I дәрежелі), өте нашар дифференциалданған жасушаларға дейін (III дәреже) дейінгі эндометрия қатерлі ісіктерін гистологиялық классификациялаудың үш деңгейлі жүйесі бар.[22] І дәрежелі қатерлі ісік аурулары ең аз агрессивті және болжам бойынша ең жақсы, ал III дәрежелі ісіктер ең агрессивті және қайталануы ықтимал. II дәрежелі қатерлі ісік аурулары жасушалардың дифференциациясы мен аурудың агрессивтілігі тұрғысынан I және III дәрежелер арасында аралық болып табылады.[54]
Эндометриялық қатерлі ісіктердің гистопатологиясы өте алуан түрлі. Ең жиі кездесетін нәтиже - бұл жақсы сараланған эндометриоидты аденокарцинома,[45] ол әртүрлі, ядролық атипия, митоздық белсенділік және стратификация деңгейіне ие көптеген шағын, толып жатқан бездерден тұрады. Бұл көбінесе эндометрия гиперплазиясының фонында пайда болады. Фрэнк аденокарциноманы типтік емес гиперплазиядан айқын стромалық инвазия немесе эндометрия стромасын қатерлі ісікпен алмастыратын «арқа-арқа» бездерін табу арқылы ажыратуға болады. Аурудың дамуымен миометрия инфильтрацияланған.[55]
Сахналау
Эндометриялық карцинома хирургиялық жолмен кезеңделеді FIGO қатерлі ісік ауруы жүйе. 2009 жылғы FIGO қойылым жүйесі келесідей:[56][57]
| Кезең | Сипаттама |
|---|---|
| IA | Ісік жатырда миометриялық инвазияның жартысынан азымен шектеледі |
| IB | Ісік жатырда миометриялық инвазияның жартысынан көбімен шектеледі |
| II | Ісікке жатыр мен жатыр мойны қатысады строма |
| IIIA | Ісік басып кіреді сероза немесе аднекса |
| IIIB | Қынаптық және / немесе параметрлік қатысу |
| IIIC1 | Жамбас лимфа түйіндерінің тартылуы |
| IIIC2 | Пара-қолқа лимфа түйіндерінің, жамбас түйіндерінің қатысуымен немесе онсыз |
| IVA | Ісік қуықтың шырышты қабығына және / немесе ішектің шырышты қабығына енеді |
| IVB | Ішкі метастаздарды және / немесе қоса, алыс метастаздар шап лимфа түйіндері |
Миометриялық инвазия және жамбас және пара-аорталық лимфа түйіндерінің қатысуы көбінесе таралу заңдылығы болып табылады.[2] Кейде 0 кезеңі қосылады, бұл жағдайда ол «деп аталадыin situ қатерлі ісігі ".[9] Болжам бойынша ерте сатыдағы қатерлі ісіктердің 26% -ында хирургиялық араласу кезінде жамбас және алыстағы метастаздар анықталды, бұл кешенді хирургиялық кезеңді жүргізуді қажет етеді.[25]

Эндометриялық қатерлі ісіктің IA және IB сатысы
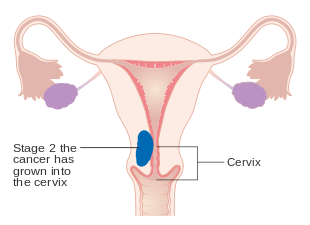
Эндометриялық қатерлі ісіктің II сатысы
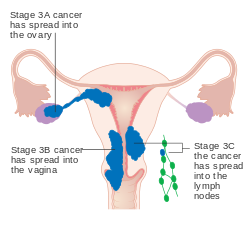
Эндометрия қатерлі ісігінің III сатысы

Эндометрия қатерлі ісігінің IV кезеңі
Басқару
Хирургия

Эндометрия обырын алғашқы емдеу хирургиялық араласу болып табылады; Эндометриялы қатерлі ісікке шалдыққан әйелдердің 90% -ы қандай-да бір хирургиялық еммен емделеді.[22] Хирургиялық емдеу әдетте тұрады гистерэктомия оның ішінде екіжақты сальпинго-оофорэктомия, бұл жатырдың және аналық бездердің де, фаллопиялық түтіктердің де алынуы. Лимфаденэктомия, немесе жамбас пен пара-қолқаны алып тастау лимфа түйіндері, гистологиялық II немесе одан жоғары дәрежелі ісіктер үшін жасалады.[16] Лимфаденэктомия АҚШ-тағы эндометриялы қатерлі ісіктің барлық сатыларында жүйелі түрде жасалады, бірақ Ұлыбританияда лимфа түйіндері әдетте тек II сатыдағы немесе одан жоғары сатыдағы аурумен жойылады.[15] Лимфаденэктомия тақырыбы және аурудың І сатысында тіршілік етудің қандай пайдасы бар деген мәселе әлі күнге дейін талқылануда.[21] Аурудың болжамды I сатысы бар әйелдерде 2017 жылғы жүйелік шолу лимфаденэктомиямен салыстырғанда лимфаденэктомияның өлім немесе қатерлі ісік ауруының қайталану қаупін төмендететініне ешқандай дәлел таппады.[58] Лимфаденэктомияға ұшыраған әйелдерде хирургиялық араласуға немесе лимфодема / лимфоциста түзілуіне байланысты жүйелі ауру байқалады.[58] Қатерлі ісіктердің III және IV сатысында, циторедуктивті хирургия бұл норма,[16] және биопсиясы omentum енгізілуі мүмкін.[59] Аурудың IV сатысында, алыстағы метастаздар болған кезде, хирургиялық араласуды паллиативті терапияның бөлігі ретінде қолдануға болады.[21] Лапаротомия, іштің ашық процедурасы, бұл дәстүрлі хирургиялық процедура; дегенмен, бастапқы эндометриялық қатерлі ісікке шалдыққан адамдарда, лапароскопия (кілт саңылауларындағы хирургия) жедел аурушаңдықтың төмендеуімен және жалпы және аурусыз өмір сүрумен байланысты.[59] Жатырдың іш қуысы арқылы алынуы ұсынылады жатырдың қынап арқылы алынуы өйткені бұл зерттеуге және алуға мүмкіндік береді жуу қатерлі ісіктің кез-келген дәлелін анықтау үшін іш қуысының. Қатерлі ісіктің сатысы хирургиялық араласу кезінде жасалады.[60]
Операцияға бірнеше қарсы көрсеткіштерге жұмыс істемейтін ісік, масылдық семіздік, ерекше қауіпті операция немесе ұрықтылықты сақтау ниеті жатады.[60] Бұл қарсы көрсеткіштер шамамен 5-10% жағдайда болады.[21] Ұрықтылығын сақтағысы келетін және І дәрежелі қатерлі ісіктің төмен дәрежелі әйелдерін прогоксиндермен емдеуді бір мезгілде тамоксифен терапиясымен немесе онсыз жүзеге асыруға болады. Бұл терапияны қатерлі ісік терапияға жауап бермейінше немесе бала көтеру аяқталғанға дейін жалғастыруға болады.[61] Жатырдың перфорациясы D&C немесе эндометрия биопсиясы кезінде пайда болуы мүмкін.[62] Эндометрияның қатерлі ісігін жою операциясының жанама әсерлері жыныстық дисфункцияны, уақытша ұстамауды және т.б. қамтуы мүмкін лимфедема, кез-келген хирургияның, соның ішінде жиі кездесетін жанама әсерлерімен бірге іш қату.[9]
Қосымша терапия
Бірқатар мүмкін болатын қосымша терапия әдістері бар. Хирургиялық араласуды жалғастыруға болады сәулелік терапия және / немесе химиотерапия жоғары қатерлі немесе жоғары дәрежелі қатерлі ісік жағдайында. Бұл деп аталады көмекші терапия.[16]
Химиотерапия
Адъювантты химиотерапия - бұл кейбір үйлесімдерден тұратын жақындағы жаңалық паклитаксел (немесе басқасы таксондар сияқты доцетаксел ), доксорубицин (және басқа да антрациклиндер ), және платиналар (әсіресе цисплатин және карбоплатин ). Адъювантты химиятерапия қатерлі ісіктің III және IV сатыларында өмір сүруді жоғарылататыны анықталды радиотерапия қосылды.[16][21][22][63] Сәйкес келмейтін жөндеу гендерінің мутациясы, Линч синдромындағы сияқты, платинаға қарсы тұруға әкелуі мүмкін, яғни бұл мутациясы бар адамдарда платиндермен химиотерапия тиімсіз.[64] Химиотерапияның жанама әсерлері жиі кездеседі. Оларға жатады шаштың түсуі, нейтрофилдердің төмен деңгейі қандағы және асқазан-ішек жолдарының проблемалары.[16]
Операция көрсетілмеген жағдайларда, паллиативті химиотерапия бұл опция; жоғары дозалы химиотерапия ұзақ өмір сүрумен байланысты.[16][22][63] Паллиативті химиотерапия, әсіресе қолдану капецитабин және гемцитабин, сонымен қатар эндометриялық қатерлі ісікті емдеу үшін жиі қолданылады.[63]
Төмен сенімділік химиотерапия алған эндометриялы қатерлі ісік ауруы бар әйелдерде mTOR жолын тежейтін дәрілерді қабылдау химиотерапиямен немесе гормоналды терапиямен салыстырғанда аурудың нашарлау қаупін төмендетуі мүмкін екенін көрсетеді. MTOR ингибиторлары асқазан-ішек жолдарының ойық жарасының пайда болу мүмкіндігін арттыруы мүмкін.[65]
Радиотерапия
Адъювантты сәулелік терапия әдетте эндометрия қатерлі ісігінің ерте сатысында (I немесе II сатысында) қолданылады. Оны вагинальды брахитерапия (VBT) арқылы жеткізуге болады, ол уыттылығының төмендеуіне байланысты қолайлы жолға айналады немесе сыртқы сәулелік сәулелік терапия (EBRT). Брахитерапия зардап шеккен органға сәулелену көзін орналастыруды қамтиды; эндометриялық қатерлі ісік жағдайында сәулелену көзі қынапқа тікелей орналастырылады. Сыртқы сәулелік сәулелік терапия дененің сыртынан зардап шеккен аймаққа бағытталған сәулелену сәулесін қамтиды. VBT кез келген қалған қатерлі ісіктерді тек қынапта емдеу үшін қолданылады, ал ЕБРТ хирургиялық араласудан кейін жамбастың басқа жерлерінде қалған қатерлі ісіктерді емдеу үшін қолданыла алады. Алайда, адъювантты сәулелік терапияның пайдасы даулы. ЕҚДБ жамбастағы рецидивтің жылдамдығын едәуір төмендетсе де, жалпы тіршілік ету және метастаз деңгейі жақсармайды.[2] VBT ЕБРР-ге қарағанда өмірдің жақсы сапасын қамтамасыз етеді.[21]
Радиотерапияны белгілі бір жағдайларда хирургиялық араласуға дейін де қолдануға болады. Операцияға дейінгі бейнелеу немесе клиникалық бағалау жатыр мойнына түскен ісікті көрсеткенде, сәулеленуді a-ға дейін беруге болады жалпы гистерэктомия орындалады.[13] Brachytherapy and EBRT can also be used, singly or in combination, when there is a contraindication for hysterectomy.[21] Both delivery methods of radiotherapy are associated with side effects, particularly in the асқазан-ішек жолдары.[2]
Hormonal therapy
Hormonal therapy is only beneficial in certain types of endometrial cancer. It was once thought to be beneficial in most cases.[2][16] If a tumor is well-differentiated and known to have progesterone and estrogen receptors, progestins may be used in treatment.[63] There is no evidence to support the use of progestagen in addition to surgery for newly diagnosed endometrial cancer.[66] About 25% of metastatic endometrioid cancers show a response to progestins. Also, endometrial stromal sarcomas can be treated with hormonal agents, including tamoxifen, гидроксипрогестерон капроаты, летрозол, мегестрол ацетаты, және medroxyprogesterone.[19] This treatment is effective in endometrial stromal sarcomas because they typically have эстроген және / немесе progestin receptors. Progestin receptors function as ісік супрессорлары in endometrial cancer cells.[67] Preliminary research and clinical trials have shown these treatments to have a high rate of response even in metastatic disease.[49]
In 2010 hormonal therapy is of unclear effect in those with advanced or recurrent endometrial cancer.[68] There is insufficient evidence to inform women considering hormone replacement therapy after treatment for endometrial cancer.[69]
Мониторинг
The tumor marker CA-125 is frequently elevated in endometrial cancer and can be used to monitor response to treatment, particularly in serous cell cancer or advanced disease.[30][39][70] Periodic MRIs or CT scans may be recommended in advanced disease and women with a history of endometrial cancer should receive more frequent pelvic examinations for the five years following treatment.[70] Examinations conducted every three to four months are recommended for the first two years following treatment, and every six months for the next three years.[21]
Women with endometrial cancer should not have routine surveillance imaging to monitor the cancer unless new symptoms appear or tumor markers begin rising. Imaging without these indications is discouraged because it is unlikely to detect a recurrence or improve survival, and because it has its own costs and side effects.[71] If a recurrence is suspected, PET/CT scanning is recommended.[21]
Болжам
Өмір сүру деңгейі
| Кезең | 5-year survival rate |
|---|---|
| I-A | 88% |
| I-B | 75% |
| II | 69% |
| III-A | 58% |
| III-B | 50% |
| III-C | 47% |
| IV-A | 17% |
| IV-B | 15% |
The five-year survival rate for endometrial adenocarcinoma following appropriate treatment is 80%.[73] Most women, over 70%, have FIGO stage I cancer, which has the best prognosis. Stage III and especially Stage IV cancers has a worse prognosis, but these are relatively rare, occurring in only 13% of cases. The median survival time for stage III–IV endometrial cancer is nine to ten months.[74] Older age indicates a worse prognosis.[16] In the United States, white women have a higher survival rate than black women, who tend to develop more aggressive forms of the disease by the time of their diagnosis.[75] Tumors with high прогестерон рецепторы expression have a good prognosis compared to tumors with low progesterone receptor expression; 93% of women with high progesterone receptor disease survived to three years, compared with 36% of women with low progesterone receptor disease.[4] Жүрек ауруы is the most common cause of death among those who survive endometrial cancer,[76] with other obesity-related health problems also being common.[77] Following diagnosis, quality of life is also positively associated with a healthy lifestyle (no obesity, high-quality diet, physical activity).[78]
Қайталану жылдамдығы
Recurrence of early stage endometrial cancer ranges from 3 to 17%, depending on primary and adjuvant treatment.[73] Most recurrences (75–80%) occur outside of the pelvis, and most occur two to three years after treatment, 64% after two years and 87% after three years.[53]
Higher-staged cancers are more likely to recur, as are those that have invaded the myometrium or cervix, or that have metastasized into the lymphatic system. Papillary serous carcinoma, clear cell carcinoma, және endometrioid carcinoma are the subtypes at the highest risk of recurrence.[22] High-grade histological subtypes are also at elevated risk for recurrence.[15]
The most common site of recurrence is in the қынап;[2] vaginal relapses of endometrial cancer have the best prognosis. If relapse occurs from a cancer that has not been treated with radiation, EBRT is the first-line treatment and is often successful. If a cancer treated with radiation recurs, pelvic exenteration is the only option for curative treatment. Palliative chemotherapy, cytoreductive surgery, and radiation are also performed.[79] Radiation therapy (VBT and EBRT) for a local vaginal recurrence has a 50% five-year survival rate. Pelvic recurrences are treated with surgery and radiation, and abdominal recurrences are treated with radiation and, if possible, chemotherapy.[21] Other common recurrence sites are the pelvic lymph nodes, para-aortic lymph nodes, peritoneum (28% of recurrences), and lungs, though recurrences can also occur in the brain (<1%), liver (7%), adrenal glands (1%), bones (4–7%; typically the осьтік қаңқа ), lymph nodes outside the abdomen (0.4–1%), spleen, and muscle/soft tissue (2–6%).[53]
Эпидемиология
2014 жылғы жағдай бойынша[жаңарту], approximately 320,000 women are diagnosed with endometrial cancer worldwide each year and 76,000 die, making it the sixth most common cancer in women.[3] It is more common in developed countries, where the lifetime risk of endometrial cancer in people born with uteri is 1.6%, compared to 0.6% in developing countries.[16] Ол орын алады in 12.9 out of 100,000 women annually in developed countries.[22]
In the United States, endometrial cancer is the most frequently diagnosed gynecologic cancer and, in women, the fourth most жалпы cancer overall,[11][19] representing 6% of all cancer cases in women.[80] In that country, as of 2014[жаңарту] it was estimated that 52,630 women were diagnosed yearly and 8,590 would die from the disease.[25] Northern Europe, Eastern Europe, and North America have the highest rates of endometrial cancer, whereas Africa and West Asia have the lowest rates. Asia saw 41% of the world's endometrial cancer diagnoses in 2012, whereas Northern Europe, Eastern Europe, and North America together comprised 48% of diagnoses.[3] Unlike most cancers, the number of new cases has risen in recent years, including an increase of over 40% in the United Kingdom between 1993 and 2013.[16] Some of this rise may be due to the increase in obesity rates in developed countries,[22] increasing life expectancies, and lower birth rates.[11] The average lifetime risk for endometrial cancer is approximately 2–3% in people with uteruses.[18] In the UK, approximately 7,400 cases are diagnosed annually, and in the EU, approximately 88,000.[21]
Endometrial cancer appears most frequently during perimenopause (the period just before, just after, and during menopause), between the ages of 50 and 65;[19] overall, 75% of endometrial cancer occurs after menopause.[2] Women younger than 40 make up 5% of endometrial cancer cases and 10–15% of cases occur in women under 50 years of age. This age group is at risk for developing ovarian cancer at the same time.[19] The worldwide медиана age of diagnosis is 63 years of age;[21] Америка Құрама Штаттарында орташа age of diagnosis is 60 years of age. White American women are at higher risk for endometrial cancer than black American women, with a 2.88% and 1.69% lifetime risk respectively.[25] Japanese-American women and American Latina women have a lower rates and Native Hawaiian women have higher rates.[29]
Зерттеу
There are several experimental therapies for endometrial cancer under research, including immunologic, hormonal, and chemotherapeutic treatments. Трастузумаб (Herceptin), an антидене against the Her2 protein, has been used in cancers known to be positive for the Her2/neu oncogene, but research is still underway. Immunologic therapies are also under investigation, particularly in uterine papillary serous carcinoma.[34]
Cancers can be analyzed using genetic techniques (including ДНҚ секвенциясы және иммуногистохимия ) to determine if certain therapies specific to mutated genes can be used to treat it. PARP ингибиторлары are used to treat endometrial cancer with PTEN mutations,[3] specifically, mutations that lower the expression of PTEN. The PARP inhibitor shown to be active against endometrial cancer is олапариб. Research is ongoing in this area as of the 2010s.[24][81][82]
Research is ongoing on the use of метформин, a diabetes medication, in obese women with endometrial cancer before surgery. Early research has shown it to be effective in slowing the rate of cancer cell proliferation.[20][33] Preliminary research has shown that preoperative metformin administration can reduce expression of tumor markers. Long-term use of metformin has not been shown to have a preventative effect against developing cancer, but may improve overall survival.[20]
Темсиролимус, an mTOR inhibitor, is under investigation as a potential treatment.[21] Research shows that mTOR inhibitors may be particularly effective for cancers with mutations in PTEN.[3] Ридафоролимус (deforolimus) is also being researched as a treatment for people who have previously had chemotherapy. Preliminary research has been promising, and a stage II trial for ridaforolimus was completed by 2013.[21] There has also been research on combined ridaforolimus/progestin treatments for recurrent endometrial cancer.[83] Бевацизумаб және тирозинкиназа ингибиторлары тежейді ангиогенез, are being researched as potential treatments for endometrial cancers with high levels of тамырлы эндотелий өсу факторы.[3] Иксабепилон is being researched as a possible chemotherapy for advanced or recurrent endometrial cancer.[83] Treatments for rare high-grade undifferentiated endometrial sarcoma are being researched, as there is no established standard of care yet for this disease. Chemotherapies being researched include doxorubicin and ifosfamide.[50]
There is also research in progress on more genes and биомаркерлер that may be linked to endometrial cancer. The protective effect of combined oral contraceptives and the IUD is being investigated. Preliminary research has shown that the левоноргестрел IUD placed for a year, combined with 6 monthly injections of гонадотропинді шығаратын гормон, can stop or reverse the progress of endometrial cancer in young women.[84] An experimental drug that combines a hormone with doxorubicin is also under investigation for greater efficacy in cancers with hormone receptors. Hormone therapy that is effective in treating breast cancer, including use of ароматаза ингибиторлары, is also being investigated for use in endometrial cancer. One such drug is анастрозол, which is currently being researched in hormone-positive recurrences after chemotherapy.[83] Research into hormonal treatments for endometrial stromal sarcomas is ongoing as well. It includes trials of drugs like мифепристон, a progestin antagonist, and аминоглутетимид and letrozole, two aromatase inhibitors.[49]
Research continues into the best imaging method for detecting and staging endometrial cancer. In surgery, research has shown that complete pelvic lymphadenectomy along with hysterectomy in stage 1 endometrial cancer does not improve survival and increases the risk of negative side effects, including lymphedema. Other research is exploring the potential of identifying the қарауыл лимфа түйіндері for biopsy by injecting the tumor with dye that shines under инфрақызыл жарық. Қарқынды модуляцияланған сәулелік терапия is currently under investigation, and already used in some centers, for application in endometrial cancer, to reduce side effects from traditional radiotherapy. Its risk of recurrence has not yet been quantified. Бойынша зерттеу гипербариялық оттегі терапиясы to reduce side effects is also ongoing. The results of the PORTEC 3 trial assessing combining adjuvant radiotherapy with chemotherapy were awaited in late 2014.[83]
There is not enough evidence to determine if people with endometrial cancer benefit from additional behavioural and life style interventions that are aimed at losing excess weight.[85]
Тарих және мәдениет
Endometrial cancer is not widely known by the general populace, despite its frequency. There is low awareness of the symptoms, which can lead to later diagnosis and worse survival.[86]
Әдебиеттер тізімі
- ^ а б c г. e f ж сағ мен "General Information About Endometrial Cancer". Ұлттық онкологиялық институт. 22 сәуір 2014. Мұрағатталды түпнұсқасынан 2014 жылдың 3 қыркүйегінде. Алынған 3 қыркүйек 2014.
- ^ а б c г. e f ж сағ мен j Kong A, Johnson N, Kitchener HC, Lawrie TA (April 2012). Kong A (ed.). "Adjuvant radiotherapy for stage I endometrial cancer". Cochrane жүйелік шолулардың мәліметтер базасы. 4 (4): CD003916. дои:10.1002/14651858.CD003916.pub4. PMC 4164955. PMID 22513918.
- ^ а б c г. e f ж сағ мен j к л м n o б q р с т сен v International Agency for Research on Cancer (2014). Дүниежүзілік қатерлі ісік туралы есеп 2014 ж. Дүниежүзілік денсаулық сақтау ұйымы. Chapter 5.12. ISBN 978-92-832-0429-9.
- ^ а б c г. e f ж "Endometrial Cancer Treatment (PDQ®)". Ұлттық онкологиялық институт. 23 сәуір 2014 ж. Мұрағатталды түпнұсқасынан 2014 жылдың 3 қыркүйегінде. Алынған 3 қыркүйек 2014.
- ^ а б "SEER Stat Fact Sheets: Endometrial Cancer". Ұлттық онкологиялық институт. Мұрағатталды түпнұсқасынан 6 шілде 2014 ж. Алынған 18 маусым 2014.
- ^ GBD 2015 аурулары мен жарақаттарының таралуы және таралуы бойынша серіктестер (қазан 2016). «1990-2015 жж. 310 ауру мен жарақаттанудың ғаламдық, аймақтық және ұлттық аурушаңдығы, таралуы және мүгедектікпен өмір сүрген жылдары: 2015 жылға арналған аурулардың ғаламдық ауыртпалығын жүйелі талдау». Лансет. 388 (10053): 1545–1602. дои:10.1016 / S0140-6736 (16) 31678-6. PMC 5055577. PMID 27733282.
- ^ GBD 2015 Mortality and Causes of Death Collaborators (October 2016). «Ғаламдық, аймақтық және ұлттық өмір сүру ұзақтығы, барлық себептерден болатын өлім және өлім-жітімнің 249 себебі бойынша өлім, 1980-2015 жж.: 2015 жылға арналған аурулардың ғаламдық ауыртпалығын жүйелі талдау». Лансет. 388 (10053): 1459–1544. дои:10.1016 / s0140-6736 (16) 31012-1. PMC 5388903. PMID 27733281.
- ^ "Defining Cancer". Ұлттық онкологиялық институт. 17 қыркүйек 2007 ж. Мұрағатталды түпнұсқасынан 2014 жылғы 25 маусымда. Алынған 10 маусым 2014.
- ^ а б c г. e f ж сағ мен "What You Need To Know: Endometrial Cancer". НКИ. Ұлттық онкологиялық институт. Архивтелген түпнұсқа 8 тамыз 2014 ж. Алынған 6 тамыз 2014.
- ^ а б c г. e f ж сағ мен j Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 823. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б c г. Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 817. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ "Uterine Cancer - Cancer Stat Facts". Көру. Алынған 3 ақпан 2019.
- ^ а б c Reynolds RK, Loar PV (2010). "Gynecology". Doherty GM-де (ред.) Current Diagnosis & Treatment: Surgery (13-ші басылым). McGraw-Hill. ISBN 978-0-07-163515-8.
- ^ Clarke MA, Long BJ, Del Mar Morillo A, Arbyn M, Bakkum-Gamez JN, Wentzensen N (September 2018). "Association of Endometrial Cancer Risk With Postmenopausal Bleeding in Women: A Systematic Review and Meta-analysis". JAMA ішкі аурулары. 178 (9): 1210–1222. дои:10.1001/jamainternmed.2018.2820. PMC 6142981. PMID 30083701.
- ^ а б c г. e f ж сағ мен j к л м Saso S, Chatterjee J, Georgiou E, Ditri AM, Smith JR, Ghaem-Maghami S (July 2011). "Endometrial cancer". BMJ. 343: d3954. дои:10.1136/bmj.d3954. PMID 21734165. S2CID 206893378.
- ^ а б c г. e f ж сағ мен j к л Galaal K, Al Moundhri M, Bryant A, Lopes AD, Lawrie TA (May 2014). «Жетілдірілген эндометрия қатерлі ісігі кезіндегі адъювантты химиотерапия». Cochrane жүйелік шолулардың мәліметтер базасы. 5 (5): CD010681. дои:10.1002 / 14651858.CD010681.pub2. PMC 6457820. PMID 24832785.
- ^ а б c г. e f Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 818. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б c г. e f Ma J, Ledbetter N, Glenn L (September 2013). "Testing women with endometrial cancer for lynch syndrome: should we test all?". Онкологиядағы алдыңғы қатарлы тәжірибеші журналы. 4 (5): 322–30. дои:10.6004/jadpro.2013.4.5.4. PMC 4093445. PMID 25032011.
- ^ а б c г. e f ж сағ мен j к л Soliman PT, Lu KH (2013). "Neoplastic Diseases of the Uterus". In Lentz GM, Lobo RA, Gershenson DM, Katz VL (eds.). Кешенді гинекология (6-шы басылым). Мосби. ISBN 978-0-323-06986-1.
- ^ а б c Sivalingam VN, Myers J, Nicholas S, Balen AH, Crosbie EJ (2014). "Metformin in reproductive health, pregnancy and gynaecological cancer: established and emerging indications". Адамның көбеюі туралы жаңарту. 20 (6): 853–68. дои:10.1093/humupd/dmu037. PMID 25013215.
- ^ а б c г. e f ж сағ мен j к л м n o б q р с т сен v Colombo N, Preti E, Landoni F, Carinelli S, Colombo A, Marini C, Sessa C (October 2013). "Endometrial cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Онкология шежіресі. 24 Suppl 6: vi33–8. дои:10.1093/annonc/mdt353. PMID 24078661.
- ^ а б c г. e f ж сағ мен Vale CL, Tierney J, Bull SJ, Symonds PR (August 2012). "Chemotherapy for advanced, recurrent or metastatic endometrial carcinoma". Cochrane жүйелік шолулардың мәліметтер базасы. 8 (8): CD003915. дои:10.1002/14651858.CD003915.pub4. PMC 7104534. PMID 22895938.
- ^ Committee on Health Care for Underserved Women (December 2011). "Health Care for Transgender Individuals: Committee Opinion No. 512". Акушерлік және гинекология. 118 (6): 1454–1458. дои:10.1097/aog.0b013e31823ed1c1. PMID 22105293. Мұрағатталды түпнұсқадан 16 желтоқсан 2014 ж.
- ^ а б Reinbolt RE, Hays JL (October 2013). "The Role of PARP Inhibitors in the Treatment of Gynecologic Malignancies". Онкологиядағы шекаралар. 3: 237. дои:10.3389/fonc.2013.00237. PMC 3787651. PMID 24098868.
- ^ а б c г. e Burke WM, Orr J, Leitao M, Salom E, Gehrig P, Olawaiye AB, Brewer M, Boruta D, Villella J, Villella J, Herzog T, Abu Shahin F (August 2014). "Endometrial cancer: a review and current management strategies: part I". Гинекологиялық онкология. 134 (2): 385–92. дои:10.1016/j.ygyno.2014.05.018. PMID 24905773.
- ^ Cheng TH, Thompson DJ, O'Mara TA, Painter JN, Glubb DM, Flach S, et al. (Маусым 2016). "Five endometrial cancer risk loci identified through genome-wide association analysis". Табиғат генетикасы. 48 (6): 667–674. дои:10.1038/ng.3562. PMC 4907351. PMID 27135401.
- ^ а б O'Mara TA, Glubb DM, Amant F, Annibali D, Ashton K, Attia J, et al. (Тамыз 2018). "Identification of nine new susceptibility loci for endometrial cancer". Табиғат байланысы. 9 (1): 3166. Бибкод:2018NatCo...9.3166O. дои:10.1038/s41467-018-05427-7. PMC 6085317. PMID 30093612.
- ^ Staley H, McCallum I, Bruce J (October 2012). "Postoperative tamoxifen for ductal carcinoma in situ". Cochrane жүйелік шолулардың мәліметтер базасы. 10: CD007847. дои:10.1002/14651858.CD007847.pub2. PMID 23076938.
There is evidence from other reports that tamoxifen increases the risk of endometrial cancer although the data presented in this review describes only 10 events occurring in 1798 participants (0.5%) after seven years of follow-up.
- ^ а б c г. "Endometrial Cancer Prevention". PDQ. NIH. 28 ақпан 2014. Мұрағатталды from the original on 5 January 2015.
- ^ а б c Coleman RL, Ramirez PT, Gershenson DM (2013). "Neoplastic Diseases of the Ovary". In Lentz GM, Lobo RA, Gershenson DM, Katz VL (eds.). Кешенді гинекология (6-шы басылым). Мосби. ISBN 978-0-323-06986-1.
- ^ Biswas A, Oh PI, Faulkner GE, Bajaj RR, Silver MA, Mitchell MS, Alter DA (January 2015). "Sedentary time and its association with risk for disease incidence, mortality, and hospitalization in adults: a systematic review and meta-analysis". Ішкі аурулар шежіресі. 162 (2): 123–32. дои:10.7326/M14-1651. PMID 25599350. S2CID 7256176.
- ^ а б Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 819. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б c г. Suh DH, Kim JW, Kang S, Kim HJ, Lee KH (July 2014). "Major clinical research advances in gynecologic cancer in 2013". Гинекологиялық онкология журналы. 25 (3): 236–48. дои:10.3802/jgo.2014.25.3.236. PMC 4102743. PMID 25045437.
- ^ а б c г. e f Thaker PH, Sood AK (1 January 2012). "Molecular Oncology in Gynecologic Cancer". In Lentz GM, Lobo RA, Gershenson DM, Katz VL (eds.). Кешенді гинекология (6-шы басылым). Мосби. ISBN 978-0-323-06986-1.
- ^ Mani RS (September 2014). "The emerging role of speckle-type POZ protein (SPOP) in cancer development". Бүгінде есірткіні табу. 19 (9): 1498–502. дои:10.1016/j.drudis.2014.07.009. PMC 4237012. PMID 25058385.
A recent exome-sequencing study revealed that 8% of serious endometrial cancers and 9% of clear cell endometrial cancers have SPOP mutations
- ^ Luo L, Luo B, Zheng Y, Zhang H, Li J, Sidell N (December 2018). "Oral and intrauterine progestogens for atypical endometrial hyperplasia". Cochrane жүйелік шолулардың мәліметтер базасы. 12: CD009458. дои:10.1002/14651858.CD009458.pub3. PMC 6517239. PMID 30521671.
- ^ Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 820. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 821. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б c г. Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 824. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б Murali R, Soslow RA, Weigelt B (June 2014). "Classification of endometrial carcinoma: more than two types". Лансет. Онкология. 15 (7): e268–78. дои:10.1016/S1470-2045(13)70591-6. PMID 24872110.
- ^ Mendivil, Alberto; Schuler, Kevin M.; Gehrig, Paola A. (2009). "Non-Endometrioid Adenocarcinoma of the Uterine Corpus: A Review of Selected Histological Subtypes". Қатерлі ісікке қарсы күрес. 16 (1): 46–52. дои:10.1177/107327480901600107. ISSN 1073-2748. PMID 19078929.
- ^ а б c г. Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 826. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б c г. e Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 827. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б Colombo N, Preti E, Landoni F, Carinelli S, Colombo A, Marini C, Sessa C (September 2011). "Endometrial cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Онкология шежіресі. 22 Suppl 6 (Supplement 6): vi35–9. дои:10.1093/annonc/mdr374. PMID 21908501.
- ^ а б Johnson N, Bryant A, Miles T, Hogberg T, Cornes P (October 2011). "Adjuvant chemotherapy for endometrial cancer after hysterectomy". Cochrane жүйелік шолулардың мәліметтер базасы (10): CD003175. дои:10.1002/14651858.CD003175.pub2. PMC 4164379. PMID 21975736.
- ^ Goodrich S, Kebria-Moslemi M, Broshears J, Sutton GP, Rose P (September 2013). "Primary squamous cell carcinoma of the endometrium: two cases and a review of the literature". Diagnostic Cytopathology. 41 (9): 817–20. дои:10.1002/dc.22814. PMID 22241749. S2CID 205746422.
- ^ Mariño-Enríquez A, González-Rocha T, Burgos E, Stolnicu S, Mendiola M, Nogales FF, Hardisson D (November 2008). т.б. "Transitional cell carcinoma of the endometrium and endometrial carcinoma with transitional cell differentiation: a clinicopathologic study of 5 cases and review of the literature". Адам патологиясы. 39 (11): 1606–13. дои:10.1016/j.humpath.2008.03.005. PMID 18620731.
- ^ Ahluwalia M, Light AM, Surampudi K, Finn CB (October 2006). "Transitional cell carcinoma of the endometrium: a case report and review of the literature". Халықаралық гинекологиялық патология журналы. 25 (4): 378–82. дои:10.1097/01.pgp.0000215296.53361.4b. PMID 16990716.
- ^ а б c Sylvestre VT, Dunton CJ (сәуір 2010). «Летрозолмен қайталанатын эндометриялы стромальды саркоманы емдеу: жағдай туралы есеп және әдебиетке шолу». Гормондар және қатерлі ісік. 1 (2): 112–5. дои:10.1007 / s12672-010-0007-9. PMID 21761354. S2CID 26057966.
- ^ а б Hensley ML (2012). "Uterine sarcomas: histology and its implications on therapy". American Society of Clinical Oncology Educational Book. Американдық клиникалық онкология қоғамы. Жылдық кездесу: 356–61. дои:10.14694/EdBook_AM.2012.32.356 (inactive 22 December 2020). PMID 24451763.CS1 maint: DOI 2020 жылғы желтоқсандағы жағдай бойынша белсенді емес (сілтеме)
- ^ D'Angelo E, Prat J (January 2010). "Uterine sarcomas: a review". Гинекологиялық онкология. 116 (1): 131–9. дои:10.1016/j.ygyno.2009.09.023. PMID 19853898.
- ^ Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 828. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ а б c Kurra V, Krajewski KM, Jagannathan J, Giardino A, Berlin S, Ramaiya N (March 2013). "Typical and atypical metastatic sites of recurrent endometrial carcinoma". Cancer Imaging. 13: 113–22. дои:10.1102/1470-7330.2013.0011. PMC 3613792. PMID 23545091.
- ^ Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 825. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ Weidner N, Coté R, Suster S, Weiss L, eds. (2002). Қазіргі хирургиялық патология (2 томдық жинақ). WB Saunders. ISBN 978-0-7216-7253-3.
- ^ "Stage Information for Endometrial Cancer". Ұлттық онкологиялық институт. Қаңтар 1980 ж. Мұрағатталды түпнұсқасынан 6 сәуір 2014 ж. Алынған 23 сәуір 2014.
- ^ Murray J. Casey; Garth K. Summers; David Crotzer. "Endometrial Cancer". StatPearls, Ұлттық биотехнологиялық ақпарат орталығы.CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме) Last Update: July 13, 2020
- ^ а б Frost JA, Webster KE, Bryant A, Morrison J (October 2017). "Lymphadenectomy for the management of endometrial cancer". Cochrane жүйелік шолулардың мәліметтер базасы. 10: CD007585. дои:10.1002/14651858.cd007585.pub4. PMC 6485923. PMID 28968482.
- ^ а б Galaal K, Bryant A, Fisher AD, Al-Khaduri M, Kew F, Lopes AD (October 2018). «Лапароскопия мен лапаротомияға қарсы эндометриялық қатерлі ісіктің ерте сатысында». Cochrane жүйелік шолулардың мәліметтер базасы. 10: CD006655. дои:10.1002 / 14651858.CD006655.pub3. PMC 6517108. PMID 30379327.
- ^ а б Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 829. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 833. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ McGee J, Covens A (2013). "Gestational Trophoblastic Disease". In Lentz GM, Lobo RA, Gershenson DM, Katz VL (eds.). Кешенді гинекология (6-шы басылым). Мосби. ISBN 978-0-323-06986-1.
- ^ а б c г. Smith JA, Jhingran A (2013). "Principles of Radiation Therapy and Chemotherapy in Gynecologic Cancer". In Lentz GM, Lobo RA, Gershenson DM, Katz VL (eds.). Кешенді гинекология (6-шы басылым). Мосби. ISBN 978-0-323-06986-1.
- ^ Guillotin D, Martin SA (November 2014). "Exploiting DNA mismatch repair deficiency as a therapeutic strategy". Эксперименттік жасушаларды зерттеу. 329 (1): 110–5. дои:10.1016/j.yexcr.2014.07.004. PMID 25017099.
- ^ Roncolato F, Lindemann K, Willson ML, Martyn J, Mileshkin L (October 2019). "PI3K/AKT/mTOR inhibitors for advanced or recurrent endometrial cancer". Cochrane жүйелік шолулардың мәліметтер базасы. 10: CD012160. дои:10.1002/14651858.cd012160.pub2. PMC 6953296. PMID 31588998.
- ^ Martin-Hirsch PP, Bryant A, Keep SL, Kitchener HC, Lilford R (June 2011). "Adjuvant progestagens for endometrial cancer". Cochrane жүйелік шолулардың мәліметтер базасы (6): CD001040. дои:10.1002/14651858.cd001040.pub2. PMC 4238061. PMID 21678331.
- ^ Patel B, Elguero S, Thakore S, Dahoud W, Bedaiwy M, Mesiano S (2014). "Role of nuclear progesterone receptor isoforms in uterine pathophysiology". Адамның көбеюі туралы жаңарту. 21 (2): 155–73. дои:10.1093/humupd/dmu056. PMC 4366574. PMID 25406186.
- ^ Kokka F, Brockbank E, Oram D, Gallagher C, Bryant A (December 2010). "Hormonal therapy in advanced or recurrent endometrial cancer". Cochrane жүйелік шолулардың мәліметтер базасы (12): CD007926. дои:10.1002/14651858.cd007926.pub2. PMC 4164823. PMID 21154390.
- ^ "Endometrial cancer risk was lower in women who used continuous combined HRT than in non-users". Evidence-based Obstetrics & Gynecology. 8 (1–2): 68–69. Наурыз 2006. дои:10.1016/j.ebobgyn.2006.01.011. ISSN 1361-259X.
- ^ а б Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, eds. (2012). "Endometrial Cancer". Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 831. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ "Five Things Physicians and Patients Should Question". Ақылды таңдау. Society of Gynecologic Oncology. 31 қазан 2013. Мұрағатталды түпнұсқадан 2013 жылғы 1 желтоқсанда. Алынған 27 шілде 2014.
- ^ "Survival by stage of endometrial cancer". Американдық онкологиялық қоғам. 2 наурыз 2014 ж. Мұрағатталды түпнұсқасынан 2014 жылғы 31 шілдеде. Алынған 10 маусым 2014.
- ^ а б Nicolaije KA, Ezendam NP, Vos MC, Boll D, Pijnenborg JM, Kruitwagen RF, Lybeert ML, van de Poll-Franse LV (May 2013). «Эндометриялы қатерлі ісік ауруының кейінгі тәжірибесі және пациенттің және аурухананың сипаттамаларымен байланысы: PROFILES популяциясының тізілімінен зерттеу». Гинекологиялық онкология. 129 (2): 324–31. дои:10.1016 / j.ygyno.2013.02.018. PMID 23435365.
- ^ Ang C, Bryant A, Barton DP, Pomel C, Naik R (February 2014). "Exenterative surgery for recurrent gynaecological malignancies". Cochrane жүйелік шолулардың мәліметтер базасы. 2 (2): CD010449. дои:10.1002/14651858.CD010449.pub2. PMC 6457731. PMID 24497188.
- ^ Soliman PT, Lu KH (2013). "Neoplastic Diseases of the Uterus". In Lentz GM, Lobo RA, Gershenson DM, Katz VL (eds.). Кешенді гинекология (6-шы басылым). Мосби. ISBN 978-0-323-06986-1.
- ^ Ward KK, Shah NR, Saenz CC, McHale MT, Alvarez EA, Plaxe SC (August 2012). «Жүрек-қан тамырлары ауруы эндометриялы қатерлі ісік аурулары арасында өлімнің негізгі себебі болып табылады». Гинекологиялық онкология. 126 (2): 176–9. дои:10.1016 / j.ygyno.2012.04.013. PMID 22507532.
- ^ Фадер А.Н., Арриба Л.Н., Фрейз ХЭ, фон Груениген В.Е. (шілде 2009). «Эндометриялық қатерлі ісік және семіздік: эпидемиология, биомаркерлер, алдын-алу және аман қалу». Гинекологиялық онкология. 114 (1): 121–7. дои:10.1016 / j.ygyno.2009.03.039. PMID 19406460.
- ^ Koutoukidis DA, Knobf MT, Lanceley A (маусым 2015). «Эндометриялық қатерлі ісіктен аман қалғандардың семіздігі, тамақтануы, физикалық белсенділігі және денсаулыққа байланысты өмір сапасы». Тамақтану туралы шолулар. 73 (6): 399–408. дои:10.1093 / nutrit / nuu063. PMC 4477700. PMID 26011914.
- ^ Hoffman BL, Schorge JO, Schaffer JI, Halvorson LM, Bradshaw KD, Cunningham FG, редакциялары. (2012). «Эндометриялық қатерлі ісік». Уильямс гинекологиясы (2-ші басылым). McGraw-Hill. б. 834. ISBN 978-0-07-171672-7. Мұрағатталды түпнұсқасынан 2014 жылғы 4 қаңтарда.
- ^ «Эндометриялық қатерлі ісік туралы жалпы ақпарат». Эндометриялық қатерлі ісікті емдеу (PDQ). NIH. 23 сәуір 2014 ж. Мұрағатталды түпнұсқасынан 2014 жылғы 20 маусымда.
- ^ Ли Дж.М., Ледерманн Дж.А., Кон EC (қаңтар 2014). «BRCA1 / 2 мутациямен байланысты және BRCA тәрізді қатерлі ісіктерге арналған PARP ингибиторлары». Онкология шежіресі. 25 (1): 32–40. дои:10.1093 / annonc / mdt384. PMC 3868320. PMID 24225019.
- ^ Банерджи С, Кайе С (желтоқсан 2011). «BRCA генінің мутациясы бар аналық без қатерлі ісігіндегі PARP ингибиторлары». Ағымдағы онкологиялық есептер. 13 (6): 442–9. дои:10.1007 / s11912-011-0193-9. PMID 21913063. S2CID 3079985.
- ^ а б c г. «Іштің қатерлі ісігін зерттеу». CancerHelp UK. Cancer Research UK. Мұрағатталды түпнұсқасынан 2014 жылғы 22 тамызда. Алынған 31 тамыз 2014.
- ^ Minig L, Franchi D, Boveri S, Casadio C, Bocciolone L, Sideri M (наурыз 2011). «Эндретриялы жатырдың алдын-алу құралдары мен жас әйелдердің жақсы сараланған ерте эндометриялы карциномасын емдеуге арналған прогестинді жатырішілік құрал және GnRH аналогы». Онкология шежіресі. 22 (3): 643–9. дои:10.1093 / annonc / mdq463. PMID 20876910.
- ^ Kitson S, Ryan N, MacKintosh ML, Edmondson R, Duffy JM, Crosbie EJ (ақпан 2018). «Эндометриялық қатерлі ісік ауруы бар әйелдердің өмір сүруін жақсарту үшін семіздіктің салмағын төмендетуге бағытталған шаралар». Cochrane жүйелік шолулардың мәліметтер базасы. 2: CD012513. дои:10.1002 / 14651858.CD012513.pub2. PMC 6491136. PMID 29388687.
- ^ Carlisle D (21 қыркүйек 2014). «Іштің қатерлі ісігі: сіз ешқашан естімеген ең кең таралған диагноз». The Guardian. Мұрағатталды түпнұсқасынан 22 қыркүйек 2014 ж. Алынған 29 қыркүйек 2014.
Сыртқы сілтемелер
| Жіктелуі | |
|---|---|
| Сыртқы ресурстар |





