Фостемсавир - Fostemsavir
 | |
 | |
| Клиникалық мәліметтер | |
|---|---|
| Сауда-саттық атаулары | Рукобия |
| Басқа атаулар | BMS-663068, GSK3684934 |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a620046 |
| Лицензия туралы мәліметтер |
|
| Жүктілік санат |
|
| Маршруттары әкімшілік | Ауыз арқылы |
| ATC коды |
|
| Құқықтық мәртебе | |
| Құқықтық мәртебе | |
| Идентификаторлар | |
| |
| CAS нөмірі | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CompTox бақылау тақтасы (EPA) | |
| Химиялық және физикалық мәліметтер | |
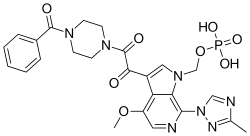
| Формула | C25H26N7O8P |
| Молярлық масса | 583.498 г · моль−1 |
| 3D моделі (JSmol ) | |
| |
| |
Фостемсавир, сауда маркасымен сатылады Рукобия, бұл АИТВ / ЖИТС-пен өмір сүретін, бірнеше рет АИТВ-мен емделген ересектерге арналған және АИВ-инфекциясын қарсыласу, төзбеушілік немесе қауіпсіздік тұрғысынан басқа терапия әдістерімен сәтті емдеу мүмкін емес антиретровирустық дәрі.[2][1]
Көбінесе жағымсыз реакция - жүрек айнуы.[2][3][1] Қатерлі реакциялардың қатарына В немесе С гепатиті вирусын жұқтырған қатысушылар арасында бауыр ферменттерінің жоғарылауы және иммундық жүйенің өзгеруі (иммундық қалпына келтіру синдромы) кірді.[2]
Фостемсавир - бұл АҚТҚ кіру ингибиторы және а есірткі темсавир (BMS-626529).[4] Фостемсавир - бұл адамның 1 типті иммунитет тапшылығы вирусы (ВИЧ-1) gp120 бағытталған тіркеме тежегіші.[5] Ол АҚШ-та медициналық қолдануға 2020 жылдың шілдесінде мақұлданды.[2][3][5]
Медициналық қолдану
Фостемсавир басқа антиретровирустықтармен біріктірілімде, АИВ-1 инфекциясын емдеуге тәжірибесі мол, есірткіге төзімді АИВ-1 инфекциясы бар ересектерде төзімділік, төзбеушілік немесе қауіпсіздікті ескере отырып, қазіргі антиретровирустық режимін бұза отырып емдеу үшін көрсетілген.[5]
Жағымсыз әсерлер
Фостемсавир АИТВ-1 инфекциясын емдеуге арналған басқа мақұлданған дәрілерге ұқсас иммунды қалпына келтіру синдромы деп аталатын ауыр жағдай тудыруы мүмкін.[3] Бұл жағдай АИТВ-1 емдеудің басында иммундық жүйе күшейіп, ағзада ұзақ уақыт бойы жасырынып келген инфекциялармен күресе бастаған кезде болуы мүмкін.[3] Басқа елеулі жанама әсерлерге жүректің электрлік белсенділігінің (QT ұзаруы) ұзаруы және гепатит В немесе С вирусымен бірге инфекцияланған науқастарда бауыр ферменттерінің жоғарылауына байланысты жүрек ырғағының проблемалары жатады.[3]
Тарих
Ол астында болды даму арқылы ViiV денсаулық сақтау / GlaxoSmithKline АИТВ-инфекциясын емдеуде қолдану үшін. Бұғаттау арқылы gp120 вирустың рецепторы, ол вирустың бастапқы CD4 + T жасушасына қосылуын және иесінің иммундық жасушасына енуін болдырмайды; оның әсер ету әдісі АҚТҚ-ға қарсы препараттар үшін бірінші болып табылады.[6] Бұл вирустық өмірлік циклдің басқа сатысына бағытталғандықтан, вирусқа шалдыққандарға төзімділігі жоғары адамдар үшін уәде береді АҚТҚ есірткілер.[7] Gp120 - бұл вирустың өте сақталған аймағы болғандықтан, препарат өзіне төзімділікті арттыра қоймайды.[8] Тергеушілер мұны анықтады энфувиртид - төзімді және ибализумаб - ВИЧ-ке төзімді конверттер Фостемсавирге сезімтал болып қала берді. Керісінше, Фостемсавирге төзімді АИТВ барлық кіру ингибиторларына сезімтал болып қала берді. Сонымен қатар, жасушаға ену үшін CD4 рецепторын қажет етпейтін ВИЧ изоляттары Фостемсавирге де сезімтал болды және вирус CD4-тәуелді болмай, тіркеме ингибиторынан қашып кете алмады. Бұрын in vitro зерттеулер көрсеткендей, Фостемсавир екеуін де тежейді CCR5 -тропикалық және CXCR4 -тропикалық АҚТҚ.[6]

Фостемсавир АҚШ-та медициналық қолдануға 2020 жылдың шілдесінде мақұлданды.[2][3][5]
Күніне екі рет ішке қабылдаған фостемсавирдің қауіпсіздігі мен тиімділігі антиретровирустық дәрі-дәрмектерге қарамастан, қанында жоғары деңгейдегі вирус (ВИЧ-РНҚ) болған, емдеуді тәжірибелі, ересек 371 қатысушының клиникалық зерттеуінде бағаланды.[2] Екі жүз жетпіс екі қатысушы негізгі сынақ қолында емделді, ал қосымша 99 қатысушы соттың басқа қолында фостемсавир қабылдады.[2][3] Қатысушылардың көпшілігі АИТВ-мен 15 жылдан астам уақыт емделді (71 пайыз), сот процедурасына кірмес бұрын бес немесе одан да көп әр түрлі АИТВ-мен емдеу режиміне ұшыраған (85 пайыз) және / немесе СПИД-ке шалдыққан (86 пайыз).[2] Соттың негізгі кохортына қатысушылар сәтсіздікке ұшыраған антиретровирустық режимнен басқа, сегіз күн ішінде күн сайын екі рет фостемсавир немесе плацебо алды.[2][3] Сегізінші күні фостемсавирмен емделген қатысушылардың плацебо қабылдағанмен салыстырғанда қанындағы АИВ-РНҚ деңгейінің едәуір төмендеуі байқалды.[2] Сегізінші күннен кейін барлық қатысушылар фостемсавирді басқа антиретровирустық препараттармен алды.[2][3] 24 аптадан кейін фостемсавир және басқа антиретровирустық препараттардан кейін қатысушылардың 53 пайызы АИТВ РНҚ-ның бәсеңдеуіне қол жеткізді, бұл жерде ВИЧ деңгейі анықталмайтын болып саналды.[2] 96 аптадан кейін қатысушылардың 60 пайызында АИТВ РНҚ-ны басу жалғасуда.[2]
Клиникалық сынақ (NCT02362503) Солтүстік Америка, Оңтүстік Америка, Еуропа, Австралия, Тайвань және Оңтүстік Африканың 23 еліндегі 108 алаңда өткізілді.[3]
АҚШ Азық-түлік және дәрі-дәрмектерді басқару (FDA) фостемсавирге өтінім берді жылдам трек, басымдықты шолу, және серпінді терапия белгілеулер.[2] FDA ViiV денсаулық сақтауына Рукобияның келісімін берді.[2]
Әдебиеттер тізімі
- ^ а б в «Рукобиа-фостемсавир трометамин таблеткасы, қабықшамен қапталған, ұзартылған шығарылым». DailyMed. 2 шілде 2020. Алынған 14 шілде 2020.
- ^ а б в г. e f ж сағ мен j к л м n o «FDA емдеу мүмкіндігі шектеулі пациенттерге жаңа ВИЧ-емдеуді мақұлдады». АҚШ-тың Азық-түлік және дәрі-дәрмек әкімшілігі (Ұйықтауға бару). 2 шілде 2020. Алынған 2 шілде 2020.
 Бұл мақалада осы қайнар көздегі мәтін енгізілген қоғамдық домен.
Бұл мақалада осы қайнар көздегі мәтін енгізілген қоғамдық домен. - ^ а б в г. e f ж сағ мен j «Есірткіге қатысты сынақтардың суреттері: Рукобия». АҚШ Азық-түлік және дәрі-дәрмектерді басқару (FDA). 2 шілде 2020. Алынған 14 шілде 2020.
 Бұл мақалада осы қайнар көздегі мәтін енгізілген қоғамдық домен.
Бұл мақалада осы қайнар көздегі мәтін енгізілген қоғамдық домен. - ^ Лай, Ен-Тинг; Ван, Дао; О'Делл, Сиджи; Доудер, Марк К .; Шён, Арне; Cheung, Crystal S. F .; Чуанг, Гво-Ю; Друз, Алиаксандр; Лин, Боб; Макки, Криша; Пенг, Дунджун (3 қаңтар 2019). «Торлы инженерия ВИЧ-1 енуінің кішігірім молекулалық ингибирленуіне мүмкіндік беретін молекулалық ерекшеліктерді анықтауға мүмкіндік береді». Табиғат байланысы. 10 (1): 47. Бибкод:2019NatCo..10 ... 47L. дои:10.1038 / s41467-018-07851-1. ISSN 2041-1723. PMC 6318274. PMID 30604750.
- ^ а б в г. «ViiV денсаулық сақтау жүйесі емделудің бірнеше нұсқасы бар ересектердегі ВИЧ-ті емдеудің бірінші класындағы Рукобия (фостемсавир) үшін АҚШ-тың FDA мақұлдауын жариялайды» (Ұйықтауға бару). ViiV денсаулық сақтау. 2 шілде 2020. Алынған 2 шілде 2020 - Business Wire арқылы.
- ^ а б АИТВ ингибиторы BMS-663068 ерте зерттеулерге жақсы көрінеді
- ^ BMS-663068 ВИЧ-тінінің ингибиторы 2b фазасын зерттеу кезінде жақсы қауіпсіздік пен тиімділікті көрсетеді
- ^ ВИЧ-1 тіркемесі ингибиторы BMS-626529, BMS-663068 алдын-ала дәрі-дәрмектің белсенді компоненті, CD4 тәуелсіз вирустарға және басқа кіру ингибиторларына төзімді АИВ-1 конверттеріне қарсы белсенділігі
Әрі қарай оқу
- Kozal M, Aberg J, Pialoux G, Cahn P, Thompson M, Molina JM және т.б. (Наурыз 2020). «Фостемсавир ересектердегі мульти дәрілік заттарға төзімді АИТВ-1 инфекциясы». Н. Энгл. Дж. Мед. 382 (13): 1232–1243. дои:10.1056 / NEJMoa1902493. PMID 32212519.
Сыртқы сілтемелер
- «Фостемсавир». Есірткі туралы ақпарат порталы. АҚШ ұлттық медицина кітапханасы.
- «Фостемсавир трометамин». Есірткі туралы ақпарат порталы. АҚШ ұлттық медицина кітапханасы.
- Клиникалық зерттеу нөмірі NCT02362503 «Тәжірибелі пациенттердегі ингибиторларды бекітуді салыстыру» үшін ClinicalTrials.gov
