Глюкокортикоидты рецепторлы селективті модулятор - Selective glucocorticoid receptor modulator - Wikipedia
| Глюкокортикоидты рецепторлы селективті модулятор | |
|---|---|
| Есірткі сыныбы | |
 | |
| Сынып идентификаторлары | |
| Синонимдер | SEGRM; SEGRA; СЕГРАМ; ДИГРА |
| Пайдаланыңыз | Ықтимал атопиялық дерматит, глаукома, катаракта, көз инфекциясы, және басқалар |
| Биологиялық мақсат | Глюкокортикоидты рецептор |
| Химиялық класс | Стероидты; стероидты емес |
| Wikidata-да | |
Глюкокортикоидты рецепторлардың селективті модуляторлары (SEGRM) және глюкокортикоидты рецепторлық агонистер (Сегралар) бұрын белгілі болды диссоциацияланған глюкокортикоидты рецепторлардың агонистері (ДИГРА) - көптеген қалауларымен бөлісуге арналған эксперименттік дәрілер класы қабынуға қарсы, иммуносупрессивті, немесе қатерлі ісік классикалық қасиеттері глюкокортикоид есірткі, бірақ сияқты жанама әсерлері аз тері атрофиясы. SEGRAM-дің қабынуға қарсы әсері туралы клиникаға дейінгі дәлелдемелер шарықтау шегіне жеткенімен,[2] қазіргі уақытта осы СЕГРАМ-дардың қатерлі ісікке тиімділігі негізінен белгісіз.
Селективті глюкокортикоидты рецепторлардың агонистері (SEGRA) тарихи және әдетте құрылымында стероидты, ал селективті глюкокортикоидты рецепторлы модуляторлары (SEGRM) әдетте стероидты емес. Глюкокортикоидты рецепторлық агонист пен модулятордың селективті аббревиатурасы СЕГРАМ.[2] Осындай бірқатар лигандтар жасалды және клиникаға дейінгі және клиникалық сынақтарда бағаланады.
SEGRAM-лар өздерінің таңдаулылығына тек ішкі жиынды қосу арқылы қол жеткізеді глюкокортикоидты рецептор әсер ету механизмдері.[3][4]
Тарих
Синтетикалық стероидтер SEGRA тәрізді қасиеттері 1990 жылдардың соңында табылған.[5] 2000 жылдардың ішінде көптеген потенциалды SEGRAM синтезделді, олардың көпшілігі стероидты емес құрылымдарға ие болды. Жылы ұялы модельдердегі in vitro зерттеулер бұл SEGRAM молекулалары глюкокортикоидты рецептор ұқсастықпен дексаметазон, сияқты күшті глюкокортикоид және қабыну медиаторларының өндірісін басу қабілеті бар интерлейкин 6 және простагландин E2.[6] Оның үстіне, in vitro нақты SEGRAM-да апоптоз пайда болуы мүмкін простата обыры[7] және лейкемия.[8]
In vivo тышқандар мен егеуқұйрықтарға жүргізілген зерттеулер жергілікті қолданылған SEGRAM тежелгенін көрсетті пероксидаза қызметі мен қалыптасуы ісіну, қабынуға қарсы белсенділіктің екі көрсеткіші, салыстырмалы түрде преднизолон. Тышқандарға немесе егеуқұйрықтарға жүйелі түрде енгізу SEGRAM-дің жедел түрде төмендеуін көрсетеді инфекциялар, ревматоидты артрит, астма және колит.[2] In vivo Қазіргі кезде белгілі бір СЕГРАМ-дар қатерлі ісік патологияларындағы классикалық глюкокортикоидқа қарағанда ұқсас әсер етуі мүмкін емес деген дәлелдер жоқ.[2] Мысалы, егеуқұйрықтардағы тері атрофиясы предризолонға қарағанда SEGRAM көмегімен жүргізілген зерттеуде айтарлықтай аз байқалды. Мапракорат, және метаболикалық салмақтың өсуі немесе жоғарылауы сияқты әсерлер қандағы глюкоза іс жүзінде болмады.[9]
Қимыл механизмі

Селективті емес глюкокортикоидтар да, селективті глюкокортикоидты рецепторлық агонисттер де байланыстыру және активтендіру арқылы жұмыс істейді. глюкокортикоидты рецептор (GR). Глюкокортикоидтардан айырмашылығы, олар ГР-ді (кем дегенде) екіге дейін жұмыс істеуге белсендіреді сигнал беру жолдар,[10] SEGRAM-лар GR-ді екі негізгі мүмкін жолдардың бірінде ғана жұмыс істейтін етіп белсендіреді.[11]
Глюкокортикоидтар болмаған кезде ГР-да орналасады цитозол кешенді белсенді емес күйде жылу шокы белоктары (HSPs) және иммунофилиндер. Глюкокортикоидтардың ГР-мен байланысуы а тудыратын рецепторды белсендіреді конформациялық өзгеріс GR-да және осылайша байланысқан HSPs диссоциациясы. Содан кейін белсендірілген GR геннің экспрессиясын екі жолдың бірі арқылы реттей алады:[10]
- Трансактивация
- Бірінші (тікелей) жол деп аталады трансактивация осылайша белсендірілген GR күңгірттенеді, болып табылады ауыстырылды ішіне ядро және нақты тізбектерімен байланысады ДНҚ деп аталады глюкокортикоидты реакция элементтері (GRE). GR / DNA комплексі төменгі ДНҚ-ға транскрипциялайтын басқа ақуыздарды қосады мРНҚ және ақыр соңында ақуыз. Глюкокортикоидтарға жауап беретін гендердің мысалдарына кодтайтындар жатады қосымшасы A1, TSC22D3 (GILZ деп те аталады), ангиотензинді түрлендіретін фермент, бейтарап эндопептидаза және басқа қабынуға қарсы ақуыздар.
- Трансрепрессия
- Екінші (жанама) жол деп аталады транспрессия, онда белсендірілген мономерлі GR басқа транскрипция факторларымен байланысады NF-κB және АП-1 және олардың мақсатты гендерінің экспрессиясын реттеуге жол бермейді. Бұл мақсатты гендер ақуыздарды кодтайды циклооксигеназа, Синтаза жоқ, фосфолипаза A2, ісік некрозының факторы, өзгертетін өсу факторы бета, ICAM-1, және басқа бірқатар қабынуға қарсы протеиндер.

Демек, глюкокортикоидтардың қабынуға қарсы әсері трансактивациядан да, трансрепрессиядан да туындайды. Керісінше, егеуқұйрықтар мен тышқандарға жүргізілген зерттеулер глюкокортикоидтардың жанама әсерлерінің басым бөлігі екенін көрсетті диабетогенді белсенділік, остеопороз, сондай-ақ тері атрофиясы негізінен трансактивациядан туындайды.[9][12][13] Трансактивациясыз трансрепрессияға қабілетті селективті глюкокортикоид көптеген қажетті терапевтік қабынуға қарсы әсерлерін сақтап, осы жағымсыз жанама әсерлерін азайтуы керек.[11]
Тек транспрессияның қабынуға қарсы реакция үшін жеткілікті болуы мүмкін екендігінің алғашқы дәлелдері a нүктелік мутация GR-дің тышқандарда GR мөлшері азайып, ДНҚ-мен байланысуына жол бермеді және сол арқылы трансактивацияны блоктайды.[14][15] Сонымен бірге бұл мутация трансрепрессияға кедергі болған жоқ. GR тіршілік ету үшін өте маңызды болғанымен, бұл тышқандар әлі де өміршең.[14] Алайда, бұл тышқандар синтетикалық глюкокортикоидты дексаметазонмен өңделгенде, глюкозаның жоғарылауы болған жоқ. Дексаметазонмен өңделген бұл тышқандар қабыну қоздырғышына төзімді болды.[15] Демек, бұл тышқандар дексаметазонның қабынуға қарсы әсеріне жауап берді, бірақ кем дегенде кейбір жанама әсерлерге төзімді болды.
Глюкокортикоидтар сияқты, SEGRAMs GR-мен байланысады және оны белсендіреді. Алайда, глюкокортикоидтардан айырмашылығы, Сегррамдар ГР-ны таңдаулы түрде терапевтік пайда әкелетіндей етіп белсендіреді. Әдетте, белгілі бір қабынуға негізделген аурулар үшін СЕГРАМ трансактивациядан гөрі күшті транспрепрессияға ие болуы керек, немесе транскрепрессияға жақсырақ және трансактивтенбеуі керек. Селективті ГР активациясының бұл түрі классикалық глюкокортикоидтармен созылмалы емдеумен пайда болатын күтілетін жанама әсерлерден азырақ болуы керек.[16]
Клиникалық зерттеулер
Үміткер қосылыстарының бірі, мапракоратпен клиникалық зерттеулердің II кезеңі (код атаулары BOL-303242-X және ZK 245186)[17]), 2009 жылдың жазында басталды. Біреуі а қос соқыр дозаны анықтау бойынша зерттеу жақпа атопиялық дерматитке қарсы Intendis, бөлігі Bayer HealthCare фармацевтика бойынша мамандандырылған дерматология.[18] III кезеңінің сынақтары 2010 жылдың қарашасында басталды офтальмологиялық тоқтата тұру катаракта операциясынан кейінгі қабынуды емдеуге арналған Бауш & Ломб.[19]
Басқа диссоциацияланған глюкокортикоидпен II фазалық сынақ fosdagrocorat (PF-04171327) (фосфат эфирі есірткі туралы дагрокат (PF-00251802)[20][21]) ревматоидты артрит үшін 2011 жылы басталған Pfizer.[22]
Осы клиникалық зерттеулердің нәтижелері әлі жария етілмеген және клиникалық қолдануға SEGRAM әлі бекітілген жоқ.
Ықтимал қосымшалар
Атопиялық дерматит (тері), ревматоидты артрит (буындар), ... сияқты созылмалы қабыну ауруларында кортикостероидтардың жанама әсерлері ұзаққа созылған емделуге байланысты проблемалы болып табылады. Сондықтан SEGRAM-ны балама жергілікті емдеу әдісі ретінде зерттеп жатыр. Кортикостероидтармен қабынуды жүйелі ұзақ мерзімді емдеу әсіресе метаболикалық жанама әсерлер тудырады, бұл ауызша СЕГРАМ-дарды дамытудың қызықты мақсаты болып табылады.[23] Селективті рецепторлық агонистер немесе модуляторлар клиникалық қолдануда классикалық кортикоидтардан гөрі жанама әсерлерді едәуір төмендететінін білу керек.
Пайдалы атрофиялық әсерлер
Глюкокортикоидтардың атрофиялық әсері әрқашан кемшілік бола бермейді. Псориаз сияқты гиперпролиферативті ауруларды емдеу осы қасиетті қолданады.[24] Мұндай жағдайларда SEGRAM-дың тиімділігі аз болар еді. Соңғы жетістіктер көрсеткендей, бұрынғы СЕГРАМ-ны қолдану арқылы GR трансрепрессиясы мен трансактивациясын жалпы бөлуге ұмтылу GR транактивациясымен ынталандырылған қабынуға қарсы гендер сияқты нюанстарға лайық. ГИЛЗ және DUSP1, маңызды рөл атқаратын сияқты.[25][26] Осыған қарамастан, осы Сегррамдардың неғұрлым таңдаулы сипаты GR-медиацияның жанама әсерлерін азайтады және клиникалық тестілеуге лайық.
Химия


Ерте SEGRA синтетикалық стероидтер болды. Мысал - RU 24858, осы типтегі алғашқы қосылыстардың бірі.[5] Көптеген жаңа SEGRA-лардың құрылымы басқа, бірақ стероидтарға ұқсастығы бензопиранохинолин А 276575 сияқты молекулаларда немесе октаидрофенантрен-2,7-диол туындыларында байқалады. Бұл қосылыстардың барлығы SEGRA қасиеттерін жасушалық немесе жануарлар модельдерінде көрсететіні көрсетілген.[3]
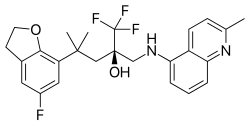
Мапракорат - стероид тәрізді құрылымы жағынан аз трифторопропаноламиндер мен -амидтердің бірі. Осы топтың басқа типтік мысалдары ZK 216348 болып табылады[9] және 55D1E1.[4] Көлемді, бициклді хош иісті алмастырғыштар (R1 және Р.2) кортикоидтарға құрылымдық ұқсастығын ескеру. The R конформация туралы асимметриялық көміртегі атомы GR-ға жақын болу үшін өте маңызды сияқты.[9]
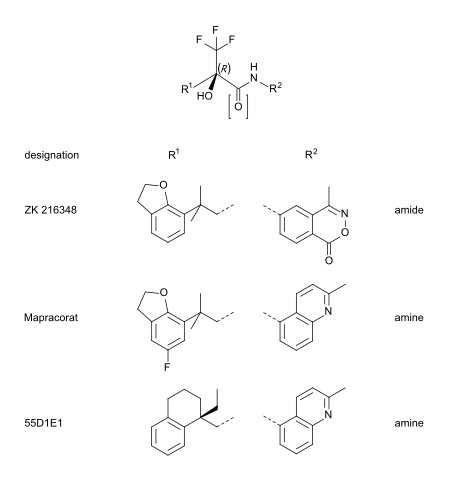
SEGRM тізімі
- Дагрокат (PF-00251802, PF-251802)
- Fosdagrocorat (PF-04171327, PF-4171327)
- Мапракорат (BOL-303242-X, ZK-245186)
Сондай-ақ қараңыз
- Селективті рецепторлық модулятор
- Селективті андрогенді рецепторлық модулятор
- Селективті рецепторлы модулятор
- Таңдамалы прогестерон рецепторларының модуляторы
Әдебиеттер тізімі
- ^ Mealy N; Dulsat C (2009). «Arbeitsgemeinschaft Dermatologische Forschung (ADF) 36-шы жылдық кездесуі». Есірткі Fut. 34 (4): 341.
- ^ а б c г. Sundahl N, Bridelance J, Libert C, De Bosscher K, Bec IM (мамыр 2015). «Глюкокортикоидты рецепторлардың селективті модуляциясы: стероидты емес тіректермен жаңа бағыттар». Фармакология және терапевтика. 152: 28–41. дои:10.1016 / j.pharmthera.2015.05.001. PMID 25958032.
- ^ а б c Робинсон Р.П., Бакбиндер Л, Хаугето А.И., МакНифф П.А., Миллхам М.Л., Риз М.Р., Шефер Дж.Ф., Абрамов Я.А., Борднер Дж, Шантиньи Я.А., Клейнман Е.Ф., Лэйрд Э.Р., Морган Б.П., Мюррей Дж.К., Салтер Э.Д., Вессель МД, Йокум С.А. (Наурыз 2009). «Октахидрофенантрен-2,7-диолдың аналогтары диссоциацияланған глюкокортикоидты рецепторлық агонистер ретінде: ашылу және қорғасынды барлау». Медициналық химия журналы. 52 (6): 1731–43. дои:10.1021 / jm801512v. PMID 19239259.
- ^ а б Biggadike K, Boudjelal M, Clackers M, Coe DM, Demaine DA, Hardy GW, Humphreys D, Inglis GG, Johnston MJ, Jones HT, House D, Loiseau R, Needham D, Skone PA, Uings I, Veitch G, Weingarten GG , McLay IM, Macdonald SJ (желтоқсан 2007). «Нестероидты емес глюкокортикоидты агонистер: диссоциацияланған (трансрепрессия / трансактивация) тиімділігі селективтілігі бар альтернативті стероидты сақиналы миметикасы бар тетрагидронафталиндер». Медициналық химия журналы. 50 (26): 6519–34. дои:10.1021 / jm070778w. PMID 18038970.
- ^ а б c Vayssière BM, Dupont S, Choquart A, Petit F, Garcia T, Marchandeau C, Gronemeyer H, Resche-Rigon M (тамыз 1997). «Трансактивацияны диссоциациялайтын синтетикалық глюкокортикоидтар және АП-1 трансрепрессиясы in vivo қабынуға қарсы белсенділік көрсетеді». Молекулалық эндокринология. 11 (9): 1245–55. дои:10.1210 / ме.11.9.1245. PMID 9259316.
- ^ а б Lin CW, Nakane M, Stashko M, Falls D, Kuk J, Miller L, Huang R, Tyree C, Miner JN, Rosen J, Kym PR, Coghlan MJ, Carter G, Lane BC (тамыз 2002). «2,5-дигидро-9-гидрокси-10-метокси-2,2,4-триметил-5- (1-метилциклогексен-3-у1) -1Н- стероидты емес глюкокортикоидты рецепторлы лигандтың транс-активтенуі және репрессиялық қасиеттері» [1] бензопирано [3,4-f] хинолин (A276575) және оның төрт стереоизомері ». Молекулалық фармакология. 62 (2): 297–303. дои:10.1124 / мол.62.2.297. PMID 12130681.
- ^ Емелянов А, Цворног Дж, Гера Л, Джоши С, Чаттертон Р.Т., Будунова I (маусым 2008). «Жаңа стероидты рецепторлық фито-модулятор қосылысы простата қатерлі ісігі жасушаларының өсуі мен тіршілігін тежейді». Онкологиялық зерттеулер. 68 (12): 4763–73. дои:10.1158 / 0008-5472.CAN-07-6104. PMID 18559523.
- ^ Лесовая Е.А., Емельянов А.Я., Кирсанов К.И., Якубовская М.Г., Будунова И.В. (2011 ж. Қараша). «Стероидты емес глюкокортикоидты рецепторлық лиганд CpdA-ның лейкемия жасушаларының CEM және K562 линияларына ісікке қарсы әсері» (PDF). Биохимия. Биохимия. 76 (11): 1242–52. дои:10.1134 / S000629791111006X. PMID 22117551. S2CID 35234449.
- ^ а б c г. Schäcke H, Schottelius A, Döcke WD, Strehlke P, Jaroch S, Schmees N, Rehwinkel H, Hennekes H, Asadullah K (қаңтар 2004). «Селективті глюкокортикоидты рецепторлық агонистің трансрепрессиядан трансактивацияның бөлінуі терапиялық эффектілерді жанама әсерлерден бөлуге әкеледі». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 101 (1): 227–32. Бибкод:2004 PNAS..101..227S. дои:10.1073 / pnas.0300372101. PMC 314167. PMID 14694204.
- ^ а б Rhen T, Cidlowski JA (қазан 2005). «Глюкокортикоидтардың қабынуға қарсы әрекеті - ескі дәрі-дәрмектерге арналған жаңа механизмдер». Жаңа Англия медицинасы журналы. 353 (16): 1711–23. дои:10.1056 / NEJMra050541. PMID 16236742.
- ^ а б Ньютон R, Холден NS (қазан 2007). «Трансрепрессия мен трансактивацияны бөлу: глюкокортикоидты рецептор үшін қайғылы ажырасу?». Молекулалық фармакология. 72 (4): 799–809. дои:10.1124 / моль.107.038794. PMID 17622575. S2CID 52803631.
- ^ Heinemann A, Schuligoi R (2008). «Глюкокортикоид - күшті және умстриттендірілген» [Глюкокортикоидтар - күшті және даулы]. Österreichische Apothekerzeitung (неміс тілінде). 62 (23).
- ^ Coghlan MJ, Jacobson PB, Lane B, Nakane M, Lin CW, Elmore SW, Kym PR, Luly JR, Carter GW, Turner R, Tyree CM, Hu J, Elgort M, Rosen J, Miner JN (мамыр 2003). «Жаңа қабынуға қарсы глюкокортикоидты тиімділікті төмендетілген жанама әсерлері сақтайды». Молекулалық эндокринология. 17 (5): 860–9. дои:10.1210 / ме.2002-0355. PMID 12586843.
- ^ а б Reichardt HM, Kaestner KH, Tuckermann J, Kretz O, Wessely O, Bock R, Gass P, Schmid W, Herrlich P, Angel P, Schütz G (мамыр 1998). «Глюкокортикоидты рецептордың ДНҚ-мен байланысуы өмір сүру үшін маңызды емес». Ұяшық. 93 (4): 531–41. дои:10.1016 / S0092-8674 (00) 81183-6. PMID 9604929. S2CID 6524157.
- ^ а б Reichardt HM, Tronche F, Bauer A, Schütz G (2000). «Cre / loxP жүйесін қолдану арқылы глюкокортикоидты сигнализацияның молекулалық-генетикалық анализі». Биологиялық химия. 381 (9–10): 961–4. дои:10.1515 / BC.2000.118. PMID 11076028. S2CID 37837380.
- ^ Schäcke H, Berger M, Rehwinkel H, Asadullah K (қыркүйек 2007). «Селективті глюкокортикоидты рецепторлық агонистер (SEGRA): терапевтік индексі жақсартылған жаңа лигандтар» (PDF). Молекулалық және жасушалық эндокринология. 275 (1–2): 109–17. дои:10.1016 / j.mce.2007.05.014. PMID 17630119. S2CID 46020217.
- ^ Cavet ME, Harrington KL, Ward KW, Zhang JZ (2010). «Мапракорат, жаңа таңдамалы глюкокортикоидты рецепторлық агонист, гиперосмолярлық индукцияланған цитокиннің бөлінуін және адамның мүйіздік эпителий жасушаларында MAPK жолдарын тежейді». Молекулалық көзқарас. 16: 1791–800. PMC 2932489. PMID 20824100.
- ^ Клиникалық зерттеу нөмірі NCT00944632 «Атопиялық дерматит кезіндегі ZK 245186 әртүрлі концентрациясының дозалық эскалациясы» үшін ClinicalTrials.gov
- ^ Клиникалық зерттеу нөмірі NCT01230125 «Катаракта операциясынан кейін көздің қабынуын емдеуге арналған мапракораттың офтальмологиялық суспензиясы» үшін ClinicalTrials.gov
- ^ Stock T, Fleishaker D, Mukherjee, A, Le V, Xu J, Zeiher B (2009). «Салауатты еріктілердегі селективті глюкокортикоидты рецепторлы модулятордың (SGRM) қауіпсіздігін, фармакокинетикасын және фармакодинамикасын бағалау». Артритті ревм. 60 (Қосымша 10): 420. дои:10.1002 / 25503-бап (белсенді емес 2020-11-09).CS1 maint: бірнеше есімдер: авторлар тізімі (сілтеме) CS1 maint: DOI 2020 жылдың қарашасындағы жағдай бойынша белсенді емес (сілтеме)
- ^ Ху X, Ду С, Тунка С, Брэден Т, Лонг KR, Ли Дж, Уэбб Э.Г., Диет Дж.Д., Хаммерт С, Роу С, Хегде СГ, Веббер РК, Обукович МГ (тамыз 2011). «Глюкокортикоидты рецепторлық лигандтардың антагонистері, бірақ ішінара емес агонистері жанама диссоциацияны көрсетеді». Эндокринология. 152 (8): 3123–34. дои:10.1210 / en.2010-1447. PMID 21558312.
- ^ Клиникалық зерттеу нөмірі NCT01393639 «Ревматоидты артрит кезінде преднизон мен плацебоға арналған эксперименттік глюкокортикоидты қосылыстың дозаларын салыстыру бойынша зерттеу» үшін ClinicalTrials.gov
- ^ Schäcke H, Hennekes H, Schottelius A, Jaroch S, Lehmann M, Schmees N, Rehwinkel H, Asadullah K (2002). «SEGRAs: қабынуға қарсы қосылыстардың жаңа класы». Эрнст Шерингтің зерттеу қорының шеберханасы (40): 357–71. дои:10.1007/978-3-662-04660-9_20. ISBN 978-3-662-04662-3. PMID 12355726.
- ^ Kerscher MJ, Hart H, Korting HC, Stalleicken D (сәуір 1995). «Мометазон фуроатының атрофогендік потенциалын in vivo бағалау, жергілікті және басқа жаңа глюкокортикоидтармен салыстырғанда жаңадан жасалған хлорланған күшті жергілікті глюкокортикоид». Халықаралық клиникалық фармакология және терапевтика журналы. 33 (4): 187–9. PMID 7620686.
- ^ Shah S, King EM, Chandrasekhar A, Newton R (мамыр 2014). «Қабыну генінің экспрессиясын және дексаметазонмен репрессияны кері байланыста бақылау кезінде митогенмен белсендірілген протеинкиназа (MAPK) фосфатаза, DUSP1 рөлі». Биологиялық химия журналы. 289 (19): 13667–79. дои:10.1074 / jbc.M113.540799. PMC 4036371. PMID 24692548.
- ^ Ayroldi E, Macchiarulo A, Riccardi C (желтоқсан 2014). «Глюкокортикоидты жанама әсерлерге бағытталған: селективті глюкокортикоидты рецепторлы модулятор немесе глюкокортикоидты индукцияланған лейцин найзағай? Перспектива». FASEB журналы. 28 (12): 5055–70. дои:10.1096 / fj.14-254755. PMID 25205742. S2CID 40874311.
