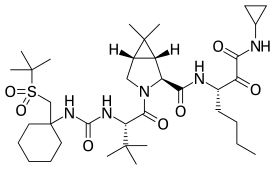
Нарлапревир - Narlaprevir
 | |
| Клиникалық мәліметтер | |
|---|---|
| Сауда-саттық атаулары | Арланса |
| Басқа атаулар | SCH 900518 |
| Маршруттары әкімшілік | Ауыз арқылы |
| ATC коды | |
| Құқықтық мәртебе | |
| Құқықтық мәртебе |
|
| Фармакокинетикалық деректер | |
| Ақуыздармен байланысуы | 86.5–91.4% |
| Метаболизм | Ауқымды бауыр тотығу, тотықсыздану және N-далькилдеу (CYP3A4 ) |
| Шығару | Нәжіс (81,1%), зәр (3,14%) |
| Идентификаторлар | |
| |
| CAS нөмірі | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ЧЕМБЛ | |
| Химиялық және физикалық мәліметтер | |
| Формула | C36H61N5O7S |
| Молярлық масса | 707.97 г · моль−1 |
| 3D моделі (JSmol ) | |
| |
| |
Нарлапревир (Сауда атауы Арланса,[1] атауымен SCH 900518),[2] болып табылады ингибитор туралы NS3 /4А серин протеазы, созылмалы емдеуге арналған гепатит С генотип 1 вирусынан туындаған) басқаларымен бірге вирусқа қарсы препараттар.[3][4][5]
Нарлапревир - созылмалы С гепатитін емдеуге арналған алғашқы ресейлік таблеткадағы дәрі.[4][6]
Қимыл механизмі
Нарлапревир - гепатит С вирусының ауызша NS3 серин протеазының ингибиторы. Ол вирусты тежейді шағылыстыру жұқтырған хостта жасушалар.[2] Ингибирлеу механизмі қайтымды болып табылады ковалентті байланыстыру NS3 протеазасы бар нарлапревир белсенді сайт арқылы кетоамид функционалдық топ.[2]
Нарлапревир адаммен байланыспайды протеаздар, қоспағанда катепсин Б. (69% ингибирлеу). Катепсин В-нің шамадан тыс экспрессиясы қатерлі ісіктердің дамуына байланысты.[7]
Пайдалану
- Көрсеткіштер
Созылмалы гепатит С вирусын (HCV) генотип 1-мен біріктіріп емдеу ритонавир, пегилирленген интерферон альфа және рибавирин, өтемақысы бар 18 жастан асқан науқастарда бауыр емдеуге бейім немесе пегилирленген интерферон альфа мен рибавириннің қосарланған қосылысы болмаған ауру. Нарлапревирді жалғыз агент ретінде пайдалану мүмкін емес.[1][2][6][8][9]
- Қарсы көрсеткіштер
Нарлапревирде кейбір қарсы көрсеткіштер бар. Соның ішінде:[1][8]
- жүктілік немесе лактация
- 18 жасқа дейінгі балалар
- ауыр нейтропения
- бауыр жеткіліксіздігі
- HCV протеаза тежегіштерімен алдын-ала емдеу
- лактаза жетіспеушілік, лактозаға төзбеушілік, глюкоза-галактозаның мальабсорбциясы.
Тиімділікті зерттеу
Х.Ризинк және басқалар. (2009) нарлапревир қауіпсіздігі мен вирусқа қарсы белсенділігін бір агент ретінде де, пегилирленген интерферон альфа-2b-мен қосарланған түрде де көрсетті.[10]
X. Тонг және басқалар. (2010) HCL-ге қарсы нарлапревир белсенділігін көрсетті мутациялар тудырады қарсылық дейін боцепревир және телапревир.[2]
2016 жылы PIONEER кең ауқымды ІІІ көп орталықты зерттеу аяқталды. Тұрақты вирусологиялық жауап (SVR) нарлапревир тобында емдеу аяқталғаннан кейін 24 аптадан соң емделуге бейім емделушілерде 89%, ал емдеу тәжірибесі бар науқастарда 70% құрады, ал бақылау тобында SVR емделушілерде тек 59,6% және 24,5% құрады. емдеу тәжірибесі бар науқастарда пегилирленген интерферон альфа және рибавиринмен қосарланған терапия. Пегилирленген интерферон альфа және рибавиринмен қосарланған терапияға нарлапревирді қосу нарлапревирдің қауіпсіздігіне әсер етпеді. Нарлапревирді зерттеудің I кезеңі фармакокинетикасы ритонавирмен бірге компенсациясы бар емделушілерде цирроз сонымен қатар аяқталды (бауырлармен кездесу AASLD, 13-17 ақпан 2015 ж., Сан-Франциско, Калифорния, АҚШ).[9][11]
Профессор И.Г. Бакулин, Мәскеудегі клиникалық зерттеу орталығының гепатология бөлімінің бастығы және Мәскеу мемлекеттік денсаулық сақтау басқармасының бас гастроэнтерологы, нарлапревирді нормативтік мақұлдау Ресейдегі гепатит С-мен күресте маңызды кезең болды.[9]
Тарих
2012 жылы R-Pharm фармацевтикалық тобы нарлапревир өндіруге лицензия алды Merck & Co. (MSD).[12] Препаратты одан әрі дамытуды R-Pharm компаниясы Техас Бауыр Институтымен (АҚШ) бірлесе отырып, «Ресей Федерациясының фармацевтикалық және медициналық индустриясын 2020 жылға дейін және одан кейінгі кезеңге дамыту» бағдарламасының қолдауымен жүргізді. .[9] Клиникалық зерттеулер мен препаратты жасауға шамамен 700 миллион рубль инвестицияланды,[4][13] оның 120 миллион рубльі Ресей үкіметінен түскен.[14]
Клиникаға дейінгі және клиникалық зерттеулер препарат Шеринг-Плоу ғылыми-зерттеу институтында (АҚШ), сонымен қатар Еуропаның бірқатар клиникалық орталықтарында өткізілді, АҚШ және Ресей.[9][13][14]
Препарат Ресейдің Ярославль қаласындағы фармацевтикалық фабрикада шығарылады.[4]
Әдебиеттер тізімі
- ^ а б c «Ресейлік дәрі-дәрмектердің мемлекеттік тіркелімі. Арланса (нарлапревир) пленкамен қапталған таблеткалар: тіркеу куәлігі» (орыс тілінде). Алынған 11 қаңтар 2017.
- ^ а б c г. e Tong X, Arasappan A, Bennett F, Chase R, Feld B, Guo Z және т.б. (Маусым 2010). «SCH 900518 (нарлапревир) вирусқа қарсы белсенділігінің клиникаға дейінгі сипаттамасы, гепатит С вирусының NS3 протеазының жаңа тежегіші тежегіші». Микробқа қарсы агенттер және химиотерапия. 54 (6): 2365–70. дои:10.1128 / AAC.00135-10. PMC 2876368. PMID 20308381.
- ^ Chen KX, Njoroge FG (2012). «12. Боцепревир мен Нарлапревирдің ашылуы: HCV NS3 протеазының ингибиторларының бірінші және екінші буыны». Хуан Х-да, Асланиан РГ (ред.). Есірткінің заманауи ашылуы мен дамуындағы жағдайлық зерттеулер. Оксфорд: Джон Вили және ұлдары, Инк., 296–335 бб. дои:10.1002 / 9781118219683.ch12. ISBN 9781118219683.
- ^ а б c г. «Российский препарат от гепатита С готовится к выпуску» (орыс тілінде). Собеседник.RU. 30 маусым 2016.
- ^ Ван Х, Генг Л, Чен Б.З., Джи М (қазан 2014). «Нарлапревирдің V36M, R155K, V36M + R155K, T54A және A156T мутацияларына байланысты HCV NS3 / 4A протеазының дәрілік заттарға төзімділігінің молекулалық механизмдерін есептеу». Биохимия және жасуша биологиясы = Biochimie et Biologie Cellulaire. 92 (5): 357–69. дои:10.1139 / bcb-2014-0039. PMID 25178998.
- ^ а б Рудакова А.В., Гусев Д.А., Усков А.Н., Коновалова Л.Н., Лобзин Ю.В. (2016). «Вирусқа қарсы препараттармен бұрын емделмеген пациенттерде созылмалы гепатит С (генотип 1) емдеудегі протеаза ингибиторларының екінші толқынының экономикалық тиімділігі». Инфекция журналы (орыс тілінде). 8 (1): 79–82. дои:10.22625/2072-6732-2016-8-1-79-82 (белсенді емес 2020-11-24).CS1 maint: DOI 2020 жылдың қарашасындағы жағдай бойынша белсенді емес (сілтеме)
- ^ Арасаппан А, Беннетт Ф, Боген SL, Венкатраман S, Блэкмен М, Чен KX және т.б. (Мамыр 2010). «Нарлапревирдің ашылуы (SCH 900518): қуатты, екінші буын HCV NS3 серин протеазының ингибиторы». ACS дәрілік химия хаттары. 1 (2): 64–9. дои:10.1021 / ml9000276. PMC 4007962. PMID 24900178.
- ^ а б Бакулин И. «Генотип 1 созылмалы гепатит С-мен ауыратын орыс пациенттеріндегі Нарлапревир» Екінші толқын «П.И.» (PDF).
- ^ а б c г. e ""R-Pharm «Нарлапревирді шығарады - С гепатитіне қарсы жаңа дәрі-дәрмек» (орыс тілінде). R-Pharm.com. 6 маусым 2016. мұрағатталған түпнұсқа 2016 жылғы 28 тамызда. Алынған 23 желтоқсан 2016.
- ^ Reesink H, Bergmann J, de Bruijne J, Weegink C, Van Lier J, Van Vliet A және т.б. (2009). «Монотерапия түрінде қолданылатын және пневинтерферон Альфа-2В-мен біріктірілген SCH 900518 қауіпсіздігі және вирусқа қарсы белсенділігі. Гепатология журналы. 50 (Жабдық 1): S35 – S36. дои:10.1016 / S0168-8278 (09) 60088-X.
- ^ Бакулин И.Г., Абдурахманов Д.Т., Богомолов П.О., Бурневич Е.З., Волошина Н.Б., Гейвандова Н.И. және т.б. «Протеаза ингибиторы Нарлапревирдің III кезеңінің алдын-ала нәтижелері, емдеуді созылмалы гепатит С генотипімен ауыратын 1-емдеу және тәжрибелік науқастар (PIONEER Study)» Тексеріңіз
| url =мәні (Көмектесіңдер) (PDF) (орыс тілінде). б. 20. - ^ Дранишникова М, Фомченко Д (21 маусым 2012). «Гепатитке қарсы бірге» (орыс тілінде). Ведомости.
- ^ а б Лапин М (30 маусым 2016). «Ресейде гепатит С препаратын өндіру басталады» (орыс тілінде).
- ^ а б Невинная И. «Минпромторг жаңа дәрі-дәрмектердің дамуын қолдайды» (орыс тілінде) (№ 5823 (150) Федералдық басылым). «Российская газета».
Әрі қарай оқу
- Бурневиш Е.З., Тихонова NY, Шаницына С.Е. (2014). «Ритонавирмен күшейтілген нарлапревир, созылмалы гепатитті емдеуде пегилирленген интерферон альфа-2А және рибавиринмен біріктірілген». Клиникалық фармакология және терапия. 5: 34–9.
