PD-L1 - PD-L1
Бағдарламаланған өлім-лиганд 1 (PD-L1) ретінде белгілі 274 (CD274) немесе B7 гомологы 1 (B7-H1) - бұл ақуыз адамдарда кодталған CD274 ген.[5]
Бағдарламаланған өлім-лиганд 1 (PD-L1) - бұл 40кДа типті 1 трансмембраналық ақуыз басуда үлкен рөл атқарады деп жорамалдаған адаптивті қолы иммундық жүйе сияқты белгілі бір оқиғалар кезінде жүктілік, тін аллографтар, аутоиммунды ауру сияқты басқа ауру күйлері гепатит. Әдетте адаптивті иммундық жүйе реакцияға түседі антигендер иммундық жүйенің экзогендік немесе эндогендік активациясымен байланысты қауіпті сигналдар. Өз кезегінде, клондық кеңеюі антиген - ерекше CD8 + T жасушалары және / немесе CD4 + көмекші ұяшықтар көбейтіледі. PD-L1 ингибиторлық бақылау нүктесінің молекуласымен байланысуы ПД-1 фосфатазалармен өзара әрекеттесуге негізделген тежегіш сигналын береді (SHP-1 немесе SHP-2 ) тирозинге негізделген иммунорецепторлы ауыстырып қосу мотиві (ITSM) арқылы.[6] Бұл лимфа түйіндерінде антигенге тән Т-жасушаларының көбеюін азайтады, сонымен бірге азайтады апоптоз реттеуші Т жасушаларында (қабынуға қарсы, супрессивті Т жасушалары) - әрі қарай геннің төменгі реттелуімен делдал болады Bcl-2.[дәйексөз қажет ]
Тарих
PD-L1 Mayo клиникасында B7-H1 иммундық реттеуші молекуласы ретінде сипатталды. Кейінірек бұл молекула PD-L1 деп өзгертілді, себебі ол PD-1 лигандасы ретінде анықталды[7] Адамның бірнеше қатерлі ісік жасушалары B7-H1 жоғары деңгейін көрсетті, ал B7-H1 блокадасы иммундық жасушалардың қатысуымен ісіктердің өсуін төмендетеді. Сол кезде В7-Н1 ісік жасушаларына ісікке қарсы иммунитеттен құтылуға көмектеседі деген қорытынды жасалды.[8] 2003 жылы B7-H1 миелоидты жасушаларда бақылау нүктесі протеині ретінде көрсетілген және адам клиникасында қатерлі ісікке қарсы иммунотерапияда потенциалды мақсат ретінде ұсынылды. [9]
Міндетті
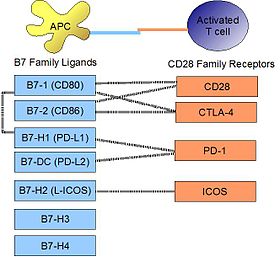
PD-L1 оның рецепторымен байланысады, ПД-1, белсендірілген Т жасушаларында, В жасушаларында және миелоидты жасушаларда, активацияны немесе тежелуді модуляциялау үшін табылған. Ретінде анықталған PD-L1 және PD-1 арасындағы жақындық диссоциация тұрақтысы Қг., 770нМ құрайды. PD-L1 сонымен қатар костимуляторлық молекулаға айтарлықтай жақындыққа ие CD80 (B7-1), бірақ жоқ CD86 (B7-2).[10] CD80-дің PD-L1, 1.4µM-ге жақындығы оның аффиниттері арасында аралық болып табылады CD28 және CTLA-4 (Сәйкесінше 4.0µM және 400nM). Байланысты молекула PD-L2 CD80 немесе CD86-ға ондай жақындығы жоқ, бірақ ПД-1-ді рецептор ретінде бөліседі (күштірек Кг. Said және басқалар. белсендірілген CD4 Т-жасушаларында жоғары реттелетін ПД-1 моноциттерде көрсетілген PD-L1-мен байланысып, соңғысының ИЛ-10 түзілуін тудыратынын көрсетті.[11]
Сигнал беру
PD-L1-ді оның рецепторымен байланыстыру ПД-1 Т жасушаларында ингибирлейтін сигнал беріледі TCR - жеделдетілген іске қосу ИЛ-2 өндіріс және Т жасушаларының көбеюі. Механизм ингибирлеуді қамтиды ZAP70 фосфорлану және оның CD3ζ.[12] ПД-1 сигналы әлсірейді PKC-θ белсендіру циклі транскрипция факторларын белсендіру үшін қажет фосфорлану (TCR сигнализациясының нәтижесінде) NF-κB және АП-1 және ИЛ-2 өндірісі үшін. PD-L1-мен байланысу сонымен бірге антигенді аңғал Т жасушаларына антигенді ұсыну кезінде лиганд индуцирленген TCR төмен модуляциясына ықпал етеді, бұл E3 ubiquitin ligase CBL-b регуляциясын индукциялау арқылы.[13]
Реттеу
Интерферондар бойынша
Кейін IFN-γ ынталандыру, PD-L1 Т жасушаларында, NK жасушаларында, макрофагтарда, миелоидты тұрақты токтарда, В жасушаларында, эпителий жасушаларында және қан тамырлары эндотелий жасушаларында көрінеді.[14] PD-L1 гендерінің промотор аймағында жауап элементі бар IRF-1, интерферонды реттеуші фактор.[15] I типті интерферондар сонымен қатар PD-L1-ді мир гепатоциттерінде, моноциттерде, тұрақты және ісік жасушаларында қалпына келтіре алады.[16]
Макрофагтар мен моноциттер туралы
PD-L1 ерекше түрде көрсетілген макрофагтар. Тінтуірде классикалық активтендірілген макрофагтар (І тип бойынша индукцияланған) көрсетілген көмекші Т жасушалары немесе комбинациясы LPS және интерферон-гамма ) PD-L1-ді айтарлықтай жаңартады.[17] Сонымен, макрофагтар арқылы белсендіріледі IL-4 (альтернативті макрофагтар), сәл PD-L1-ді жаңартыңыз, ал PD-L2-ді жаңартыңыз. Ол көрсеткен STAT1 - жетіспейтін тышқандар, бұл STAT1 көбінесе макрофагтардағы LPS немесе интерферон-гамма арқылы регуляцияға жауап береді, бірақ бұл тышқандарда активацияға дейін оның құрылымдық көрінісі үшін мүлдем жауап бермейді, сонымен қатар PD-L1 көрсетілген Ly6C тінтуірінде анықталғанміне классикалық емес моноциттер тұрақты күйде [18]
МикроРНҚ-ның рөлі
Адамға демалу холангиоциттер арқылы трансляциялық басылуына байланысты ақуызды емес, PD-L1 mRNA-ны экспрессиялаңыз микроРНҚ miR-513.[19] Интерферон-гаммамен емдеу кезінде miR-513 төмен реттелді, осылайша PD-L1 ақуызының супрессиясы көтерілді. Осылайша, интерферон-гамма мРНҚ трансляциясының гендермен басылуын тежеу арқылы PD-L1 ақуыз экспрессиясын тудыруы мүмкін. Эпштейн-Барр вирустық (EBV) жасырын мембраналық протеин-1 (LMP1) PD-L1-нің белгілі индукторы болса, EBV miRNA miR-BamH1 фрагменті H оңға қарай ашық оқудың жақтауы 1 (BHRF1) 2-5p көрсетілген. LMP1 индуцирленген PD-L1 өрнегін реттейді.[20]
Эпигенетикалық реттеу
PD-L1 промоторы ДНҚ метилденуі операциядан кейін кейбір қатерлі ісіктерде тіршілік етуді болжай алады.[21]
Клиникалық маңызы
Қатерлі ісік

PD-L1 реттелуі қатерлі ісіктердің иммундық жүйені болдырмауға мүмкіндік беруі мүмкін. Пациенттерден алынған 196 ісік үлгісін талдау бүйрек жасушалық карциномасы PD-L1 жоғары ісік экспрессиясы ісіктің агрессивтілігінің жоғарылауымен және өлім қаупінің 4,5 есе артуымен байланысты екенін анықтады.[22]Көптеген PD-L1 ингибиторлары иммуно-онкологиялық терапия ретінде дамып келеді және клиникалық зерттеулерде жақсы нәтижелер көрсетіп отыр.[23] Клиникалық қол жетімді мысалдарға мыналар жатады Дурвалумаб, пембролизумаб, атезолизумаб және авелумаб.[24]Қалыпты тіндерде STAT3 және NF-κB сияқты транскрипция факторлары арасындағы кері байланыс хост тінін қорғау және қабынуды шектеу үшін иммундық реакцияны шектейді. Қатерлі ісік кезінде транскрипция факторлары арасындағы кері байланысты шектеуді жоғалту жергілікті PD-L1 экспрессиясының жоғарылауына әкелуі мүмкін, бұл PD-L1-ге бағытталған агенттермен жүйелі емдеудің тиімділігін шектеуі мүмкін.[25]
Листерия моноцитогендері
Жасушаішілік инфекцияның тышқан моделінде, Моноцитогендер Т-жасушаларында, NK жасушаларында және макрофагтарда индукцияланған PD-L1 ақуыз экспрессиясы. PD-L1 блокадасы (блоктаушы антиденелерді қолдану) жұқтырған тышқандар үшін өлімнің жоғарылауына әкелді. Блокада TNFα және азот оксидінің макрофагтармен түзілуін, N гранзимінің NK жасушаларының түзілуін және пролиферацияның төмендеуін азайтады Моноцитогендер антигенге тән CD8 Т жасушалары (бірақ CD4 Т жасушалары емес).[26] Бұл дәлелдер PD-L1 жасуша ішілік инфекция кезінде оң костимуляторлы молекула ретінде әрекет етеді.
Аутоиммунитет
PD-1 / PD-L1 өзара әрекеттестігі бірнеше дәлелдер аутоиммунитетіне байланысты. NOD тышқандары, I типті қант диабетінің және басқа аутоиммунды аурулардың өздігінен дамуына сезімталдықты көрсететін аутоиммунитетке арналған жануарлар моделі, PD-1 немесе PD-L1 блокадасынан туындаған қант диабетінің басталуын дамытады (бірақ PD-L2 емес).[27]
Адамдарда PD-L1 педиатриялық науқастарда экспрессияның өзгергені анықталды Жүйелі қызыл жегі (SLE). Оқшауланған оқу PBMC жетілмеген балалардан миелоидты дендритті жасушалар және моноциттер бастапқы оқшаулау кезінде аз PD-L1 көрсетті, бірақ 24 сағат ішінде өздігінен жоғары реттелетін PD-L1. Керісінше, белсенді SLE-мен ауыратын науқастардың mDC-і де, моноциттері де 5-күндік уақыт ішінде PD-L1-ді қалпына келтіре алмады, бұл ақуызды аурудың ремиссиясы кезінде ғана білдірді.[28] Бұл SLE-де перифериялық төзімділікті жоғалтатын механизмдердің бірі болуы мүмкін.
Сондай-ақ қараңыз
Пайдаланылған әдебиеттер
- ^ а б c GRCh38: Ансамбльдің шығарылымы 89: ENSG00000120217 - Ансамбль, Мамыр 2017
- ^ а б c GRCm38: Ансамбльдің шығарылымы 89: ENSMUSG00000016496 - Ансамбль, Мамыр 2017
- ^ «Адамның PubMed анықтамасы:». Ұлттық биотехнологиялық ақпарат орталығы, АҚШ Ұлттық медицина кітапханасы.
- ^ «Mouse PubMed анықтамасы:». Ұлттық биотехнологиялық ақпарат орталығы, АҚШ Ұлттық медицина кітапханасы.
- ^ «Entrez Gene: CD274 CD274 молекуласы».
- ^ Chemnitz JM, Parry RV, Nichols KE, June CH, Riley JL (шілде 2004). «SHP-1 және SHP-2 иммунорецепторлық тирозинге негізделген коммутатордың өлімінің 1 бағдарламаланған өлімімен байланысады, бірақ адамның Т жасушасын алғашқы стимуляциялау кезінде, бірақ тек рецепторлардың байлауы Т жасушаларының активтенуіне жол бермейді». Иммунология журналы. 173 (2): 945–54. дои:10.4049 / jimmunol.173.2.945. PMID 15240681.
- ^ Dong H, Zhu G, Tamada K, Chen L (желтоқсан 1999). «B7-отбасының үшінші мүшесі B7-H1, Т-жасушаларының көбеюін және интерлейкин-10 секрециясын бірге ынталандырады». Табиғат медицинасы. 5 (12): 1365–9. дои:10.1038/70932. PMID 10581077. S2CID 21397460.
- ^ Dong H, Strome SE, Salomao DR, Tamura H, Hirano F, Flies DB, Roche PC, Lu J, Zhu G, Tamada K, Lennon VA, Celis E, Chen Chen (тамыз 2002). «Ісікпен байланысты B7-H1 Т-жасушалық апоптозға ықпал етеді: иммунитеттен жалтарудың ықтимал механизмі». Табиғат медицинасы. 8 (8): 793–800. дои:10.1038 / nm730. PMID 12091876. S2CID 27694471.
- ^ Кюриэль Т.Дж., Вей С, Донг Х, Альварес Х, Ченг П, Моттрам П, Кзишиек Р, Кнутсон КЛ, Даниэль Б, Циммерманн MC, Дэвид О, Буров М, Гордон А, Дурандарх Н, Майерс Л, Берггрен Р, Хемминки А , Альварес РД, Эмили Д, Кюриэль Д.Т., Чен Л, Зоу В (мамыр 2003). «B7-H1 блокадасы миелоидты дендритті жасуша-ісікке қарсы иммунитетті жақсартады». Табиғат медицинасы. 9 (5): 562–7. дои:10.1038 / nm863. PMID 12704383. S2CID 12499214.
- ^ Butte MJ, Peña-Cruz V, Kim MJ, Freeman GJ, Sharpe AH (тамыз 2008). «Адамның PD-L1 және B7-1 өзара әрекеттесуі». Молекулалық иммунология. 45 (13): 3567–72. дои:10.1016 / j.molimm.2008.05.014. PMC 3764616. PMID 18585785.
- ^ SA, Dupuy FP, Trautmann L, Zhang Y, Shi Y, El-Far M, Hill BJ, Noto A, Ancuta P, Peretz Y, Fonseca SG, Van Grevenynghe J, Boulassel MR, Bruneau J, Shoukry NH, Routy JP , Douek DC, Haddad EK, Sekaly RP (сәуір, 2010). «Моноциттерден болатын өлім-1 индуцирленген интерлейкин-10 өндірісі ВИЧ-инфекциясы кезінде CD4 + T жасушаларының активтенуін нашарлатады». Табиғат медицинасы. 16 (4): 452–9. дои:10.1038 / нм.2106. PMC 4229134. PMID 20208540.
- ^ Sheppard KA, Fitz LJ, Lee JM, Benander C, George JA, Wooters J, Qiu Y, Jussif JM, Carter LL, Wood CR, Chaudhary D (қыркүйек 2004). «ПД-1 ZAP70 / CD3zeta сигналосомасының Т-жасушалық индукцияланған фосфорлануын және PKCtheta-ға сигнал беруді тежейді». FEBS хаттары. 574 (1–3): 37–41. дои:10.1016 / j.febslet.2004.07.083. PMID 15358536. S2CID 85034305.
- ^ Karwacz K, Bricogne C, MacDonald D, Arce F, Bennett CL, Collins M, Escors D (қазан 2011). «PD-L1 ко-ынталандыру CD8 + T жасушаларында лиганд индуцирленген Т-жасуша рецепторларының төмен модуляциясына ықпал етеді». EMBO молекулалық медицина. 3 (10): 581–92. дои:10.1002 / emmm.201100165. PMC 3191120. PMID 21739608.
- ^ Flies DB, Chen L (сәуір, 2007). «Жаңа B7: ісік иммунитетінде шешуші рөл ойнайды». Иммунотерапия журналы. 30 (3): 251–60. дои:10.1097 / CJI.0b013e31802e085a. PMID 17414316.
- ^ Ли СЖ, Джанг BC, Ли SW, Ян YI, Suh SI, Park YM, Oh S, Shin JG, Yao S, Chen L, Choi IH (ақпан 2006). «Интерферонды реттеуші фактор-1 - бұл B7-H1 (CD274) құрылтай экспрессиясының және IFN-гамма-индукцияланған регуляциясының алғышарты». FEBS хаттары. 580 (3): 755–62. дои:10.1016 / j.febslet.2005.12.093. PMID 16413538. S2CID 11169726.
- ^ Yamazaki T, Akiba H, Iwai H, Matsuda H, Aoki M, Tanno Y, Shin T, Tsuchiya H, Pardoll DM, Okumura K, Azuma M, Yagita H (қараша 2002). «Мурин Т-жасушалары және АПК-пен 1 лиганд бағдарламаланған өлімнің көрінісі». Иммунология журналы. 169 (10): 5538–45. дои:10.4049 / jimmunol.169.10.5538. PMID 12421930.
- ^ Лок П, Эллисон Дж.П. (сәуір 2003). «PD-L1 және PD-L2 Th1 және Th2 жасушаларымен дифференциалды реттеледі». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 100 (9): 5336–41. дои:10.1073 / pnas.0931259100. PMC 154346. PMID 12697896.
- ^ Бианчини М, Дючене Дж, Сантовито Д, Шлосс МЖ, Эврард М, Винкельс Х, Аслани М, Моханта СК, Хоркманс М, Бланшет Х, Лэйси М, фон Хундельшаузен П, Атцлер Д, Хабенихт А, Гердес Н, Пелисек Дж, Нг LG, Steffens S, Weber C, Megens RT (маусым 2019). «Классикалық емес моноциттердегі PD-L1 экспрессиясы олардың шығу тегі мен иммунореттеу функциясын көрсетеді». Ғылыми иммунология. 4 (36): eaar3054. дои:10.1126 / sciimmunol.aar3054. PMID 31227596. S2CID 195259881.
- ^ Gong AY, Чжоу R, Ху G, Ли X, Splinter PL, O'Hara SP, LaRusso NF, Soukup GA, Dong H, Chen XM (ақпан 2009). «MicroRNA-513 B7-H1 трансляциясын реттейді және холангиоциттердегі IFN-гамма-индуцирленген B7-H1 экспрессиясына қатысады». Иммунология журналы. 182 (3): 1325–33. дои:10.4049 / jimmunol.182.3.1325. PMC 2652126. PMID 19155478.
- ^ Cristino AS, Nourse J, West RA, Sabdia MB, Law SC, Gunawardana J, Vari F, Mujaj S, Thillaiyampalam G, Snell C, Gough M, Keane C, Gandhi MK (желтоқсан 2019). «EBV microRNA-BHRF1-2-5p иммундық бақылау пункті PD-L1 және PD-L2 3'UTR-ге бағытталған». Қан. 134 (25): 2261–2270. дои:10.1182 / қан.2019000889. PMC 6923667. PMID 31856276.
- ^ Гевенслебен Х, Холмс Е.Е., Гольц Д, Дитрих Дж, Сейлор V, Эллингер Дж, Дитрих Д, Кристиансен Г (қараша 2016). «PD-L1 промотор метилизациясы - простатэктомиядан кейінгі қуық асты безінің қатерлі ісігіндегі науқастарда биохимиялық рецидивсіз тіршілік ету үшін болжамды биомаркер». Oncotarget. 7 (48): 79943–79955. дои:10.18632 / oncotarget.13161. PMC 5346762. PMID 27835597.
- ^ Томпсон РХ, Гиллетт MD, Чевилл JC, Лохсе CM, Dong H, Вебстер WS, Krejci KG, Lobo JR, Sengupta S, Chen L, Zincke H, Blute ML, Strome SE, Leibovich BC, Kwon ED (желтоқсан 2004). «Бүйрек жасушалы карциномасы бар науқастарда костимуляторлы B7-H1: ісік агрессивтілігі және потенциалды терапевтік мақсат». Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 101 (49): 17174–9. дои:10.1073 / pnas.0406351101. PMC 534606. PMID 15569934.
- ^ Velcheti V, Schalper KA, Carvajal DE, Anagnostou VK, Syrigos KN, Sznol M, Herbst RS, Gettinger SN, Chen L, Rimm DL (қаңтар 2014). «Өкпенің кіші жасушалы емес қатерлі ісігі кезіндегі өлім лиганд-1 экспрессиясы». Зертханалық зерттеу; Техникалық әдістер мен патология журналы. 94 (1): 107–16. дои:10.1038 / labinvest.2013.130. PMC 6125250. PMID 24217091.
- ^ «Қатерлі ісік ауруын емдеуге арналған иммундық бақылау тежегіштері». www.cancer.org. Алынған 2017-03-27.
- ^ Vlahopoulos, SA (15 тамыз 2017). «Қатерлі ісіктердегі NF-κB аберрантты бақылау транскрипциялық және фенотиптік икемділікке, иесінің тініне тәуелділікті азайтуға мүмкіндік береді: молекулалық режим». Қатерлі ісік биологиясы және медицина. 14 (3): 254–270. дои:10.20892 / j.issn.2095-3941.2017.0029. PMC 5570602. PMID 28884042.
- ^ Seo SK, Jeong HY, Park SG, Lee SW, Choi IW, Chen L, Choi I (қаңтар 2008). «Эндогенді B7-H1 блокадасы алғашқы Listeria monocytogenes инфекциясынан кейін бактерияға қарсы қорғанысты басады». Иммунология. 123 (1): 90–9. дои:10.1111 / j.1365-2567.2007.02708.x. PMC 2433284. PMID 17971153.
- ^ Ансари МДж, Салама А.Д., Читнис Т, Смит РН, Ягита Н, Акиба Х, Ямазаки Т, Азума М, Иваи Х, Хури СЖ, Аучинслос Х, Сайег МХ (шілде 2003). «Бағдарламаланған өлім-1 (ПД-1) жолы семіздік диабеттік тышқандардағы аутоиммунды диабетті реттейді». Тәжірибелік медицина журналы. 198 (1): 63–9. дои:10.1084 / jem.20022125. PMC 2196083. PMID 12847137.
- ^ Mozaffarian N, Wiedeman AE, Stevens AM (қыркүйек 2008). «Белсенді жүйелік қызыл жегі қызылиегі антигенді ұсынатын жасушалардың лиганд-1 өлімін білдіре алмауымен байланысты». Ревматология. 47 (9): 1335–41. дои:10.1093 / ревматология / ken256. PMC 2722808. PMID 18650228.
Сыртқы сілтемелер
- CD274 + ақуыз, + адам АҚШ ұлттық медицина кітапханасында Медициналық тақырып айдарлары (MeSH)
- Сайтында қол жетімді барлық құрылымдық ақпаратқа шолу PDB үшін UniProt: Q9NZQ7 (Бағдарламаланған жасуша өлімі 1 лиганд 1) at PDBe-KB.




