Асимметриялық гидрлеу - Asymmetric hydrogenation
Асимметриялық гидрлеу Бұл химиялық реакция екі атомын қосады сутегі екі жақтың біреуіне жақсырақ қанықпаған субстрат молекуласы, мысалы алкен немесе кетон. Селективтілік субстраттың хиралмен байланысу тәсілінен шығады катализаторлар. Жаргонмен бұл байланыс кеңістіктік ақпаратты жібереді (химиктер оны не деп атайды) ширализм ) катализатордан мақсатқа дейін, өнімді біртұтас етіп қолдайды энантиомер. Бұл «фермент сияқты селективтілік »кейбір коммерциялық синтезге қолданыладыфармацевтикалық агенттер және агрохимикаттар.

Тарих
1956 жылы а гетерогенді жасалған катализатор палладий асимметриялық гидрогенизацияға әсер ететіні жібекке қойылды.[1] Кейінірек, 1968 ж Уильям Ноулз және Леопольд Хорнер а-ны қолданып, асимметриялық гидрлеу мысалдарын өз бетінше жариялады біртекті катализаторлар. Көрмеге тек қарапайым энантиомерлі артық, бұл ерте реакциялар орындылығын көрсетті. 1972 жылға қарай энантиомерлі артық 90% -ке қол жеткізілді, ал бірінші өнеркәсіптік синтез Паркинсон есірткі L-DOPA осы технологияны қолдану арқылы басталды.[2][3]

Асимметриялық гидрогенизация өрісі бірқатар елеулі жетістіктерді бастан кешірді. Анри Каган дамыған DIOP, оңай дайындалған C2- белгілі реакцияларда жоғары эне сезімін беретін симметриялы дифосфин. Ryōji Noyori таныстырды рутений - кетондар мен альдегидтер сияқты асимметриялық гидрленген полярлы субстраттардың негізіндегі катализаторлар. Енгізу P, N лигандары содан кейін С аясын одан әрі кеңейтті2- симметриялы лигандалар, бірақ олар хиральды лигандалардан жетіспейтін дәрежеде айналу симметриясы.[4] Қазіргі кезде асимметриялық гидрлеу - бұл зертханалық және өндірістік ауқымдағы органикалық химияның күнделікті әдістемесі.
Асимметриялық гидрлеудің маңыздылығы 2001 ж Химия саласындағы Нобель сыйлығы марапатталды Уильям Стэндиш және Ryōji Noyori.
Механизм
Ішкі сала механизмдері
Екі негізгі механизмдері бар каталитикалық гидрлеу үшін ұсынылған родий кешендер: қанықпаған механизм және дигидридтік механизм. Екі механизмнің аражігін ажырату қиын болғанымен, асимметриялық гидрлеу үшін екеуінің арасындағы айырмашылық салыстырмалы түрде маңызды емес, өйткені кез-келген стереохимиялық ақпарат өнім молекуласына ауысқанға дейін екеуі де ортақ аралыққа ауысады.[5]
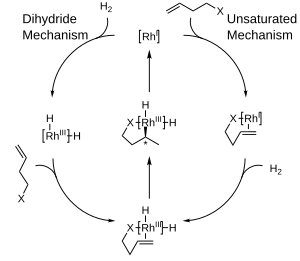
Бұл реакцияларда бір энантиомердің орнына екіншісінің орнына өндірудің артықшылығы жиі түсіндіріледі стерикалық арасындағы өзара байланыс лиганд және прохиралды субстрат. Осы өзара әрекеттесулерді қарастыру квадрант диаграммаларын жасауға әкелді, онда «бұғатталған» аймақтар көлеңкелі қораппен белгіленеді, ал «ашық» аймақтар толтырылмай қалады. Үлгіленген реакцияда кіріс тобы бойынша үлкен топтар олефин диаграмманың ашық жерлерін толтыруға бағытталады, ал кіші топтар бұғатталған жерлерге бағытталады, содан кейін олефиннің артқы жағында сутегі жеткізіліп, стереохимия. Анық болу үшін хираль фосфин лигандының тек бір бөлігі көрсетілгенін ескеріңіз.

Металдар
Платина тобындағы металдар
Родий, біртекті асимметриялық гидрлеуде қолданылатын алғашқы металл,[6] кеңінен қолданылуда. Родиймен асимметриялық гидрлеудің мақсаттары, әдетте, жақын координациялық топты қажет етеді олефин.[5] Бұл талап шектеулі болғанымен, көптеген субстрат кластары осындай функционалдандыруды иеленеді, мысалы. қанықпаған амидтер.[7]
The Ноори асимметриялық гидрлеу негізделген рутений.[8][9] Кейінгі жұмыс Нооридің катализаторлық шаблонында кеңейіп, дәстүрлі қиын субстраттардың қосылуына әкелді. т- бутил кетондар[10] және 1-тетралондар[11] рутений катализаторларымен гидрлеу үшін өміршең субстраттар ретінде. Ru және Ts негізінде гидрогенизацияны беріңізDPEN коммерциялық сәттілікке де ие болды.[12]
Иридиум катализаторлар Ru және Rh-мен жақсы катализаторлар табылмаған бірқатар «дәстүрлі емес» субстраттар үшін пайдалы.[13] Функционалды емес олефиндер[14] бұл архетиптік жағдай, бірақ басқа мысалдар, соның ішінде кетондар[15][16] бар. Иридий негізіндегі катализатордың жалпы қиындықтары олардың бейімділігі болып табылады тримеризациялау ерітіндіде.[16] Пайдалану үйлестірмейтін анион BArF
4− жинақтау мәселесінің ең кең қолданылатын шешімі болып шықты.[16][17] Катализатор тұрақтылығын күшейтудің басқа стратегияларына хирал лигандына қосымша үйлестіруші қолдың қосылуы жатады,[15] лигандтың стерикалық бөлігін ұлғайту,[18] пайдалану дендримериялық лиганд,[19] лигандтың қаттылығын арттыру,[20] лигандты иммобилизациялау,[21] және гетеробиметалл жүйелерін қолдану (металдардың бірі ретінде иридий бар).[21]
Негізгі металдар
Темір көптеген каталитикалық процестерге танымал зерттеу нысаны болып табылады, бұл оның арзан және басқа өтпелі металдарға қарағанда төмен уыттылығына байланысты.[22] Темірді қолданатын гидрлеудің асимметриялық әдістері жүзеге асырылды, дегенмен жылдамдығы мен таңдамалылығы жағынан олар қымбат металдарға негізделген катализаторлардан төмен.[23] Кейбір жағдайларда құрылымдық тұрғыдан анықталмаған нанобөлшектер өздерін белсенді түрлер ретінде дәлелдеді орнында және байқалатын қарапайым селективтілік олардың бақыланбайтын геометриялары нәтижесінде пайда болуы мүмкін.[24]
Лиганд сабақтары
Фосфин лигандары
Ширал фосфин лигандтар, әсіресе C2-симметриялық лигандалар, асимметриялық гидрлеу катализаторларының көпшілігінде хиральдылықтың көзі болып табылады. Олардың ішінен BINAP лиганд танымал болды, нәтижесінде оның Нобель сыйлығын иеленуінің нәтижесінде Ноори асимметриялық гидрлеу.[2]
Ширал фосфинді лигандтарды негізінен жіктеуге болады моно- немесе битант. Оларды стереогенді орталықтың - фосфордың және органикалық алмастырғыштардың орналасуына қарай жіктеуге болады. C бар лигандалар2 Симметрия элементі әсіресе танымал болды, өйткені мұндай элементтің болуы субстраттың метал-лигандтық кешенге байланысты байланысын күрт төмендетеді (көбінесе ерекше энансиоэлектрлікке әкеледі).[25]
Монодентатты фосфиндер
Асимметриялық гидрлеуде алғашқылардың бірі болып монофосфин типті лигандтар пайда болды, мысалы, CAMP лиганд.[26] Лигандтардың осы түрлеріне арналған зерттеулердің екеуі де зерттелді P-алкил және P-гетероатомды байланысқан лигандтар, с P-фетфатиттер тәрізді лигандар фосфорамидиттер жалпы әсерлі нәтижелерге қол жеткізу.[27] Табысты болған лигандтардың құрылымдық кластарына MonoPHOS-тың бинаптилдік құрылымына негізделгендер жатады [28] немесе SiPHOS спиро сақина жүйесі.[29] Атап айтар болсақ, бұл монодентатты лигандтарды энансиоэлектрліктің синергетикалық жақсаруына қол жеткізу үшін бір-бірімен бірге қолдануға болады;[30] мүмкін емес нәрсе дифосфинді лигандтар.[27]
Хирал дифосфинді лигандалар
Дифосфинді лигандтар монофосфиндерге қарағанда едәуір көбірек көңіл бөлді және соның салдарынан жетістік тізімі әлдеқайда ұзын болды. Бұл сыныпқа жоғары селективтілікке жететін бірінші лиганд кіреді (DIOP ), өндірістік асимметриялық синтезде қолданылатын бірінші лиганд (DIPAMP[31][32][3]) және ең танымал хираль лигандының қандай болуы мүмкін (BINAP).[2] Химальді дифосфин лигандары қазір барлық жерде асимметриялық гидрлеуде болады.

P, N және P, O лигандары


Асимметриялық гидрлеуде P, N лигандтарын қолдануды С-ге дейін анықтауға болады2 симметриялы бисоксазолинді лиганд.[33] Алайда, көп ұзамай бұл симметриялы лигандалар мономен алмастырылдыоксазолин С жетіспейтін лигандтар2 симметрия олардың асимметриялық катализдегі тиімділігін ешқандай жолмен шектемейді.[34] Мұндай лигандтар, әдетте, құрамында фитфоры бар аспалы қолмен функционалданған, құрамында гетероциклдің табиғаты мен фосфор орталығының химиялық ортасы әр түрлі болғанымен, құрамында азот бар гетероцикл бар. Ешқандай құрылым субстраттардың кең ауқымымен үнемі тиімді бола алмады, бірақ олар белгілі артықшылықты құрылымдар (фосфин-оксазолин немесе сияқты PHOX сәулет) орнатылды.[14][34][35] Сонымен қатар, сирек анықталған субстрат класы шеңберінде хиральды P, N лигандары бар металл кешендерінің өнімділігі мақсатқа жету өте қиын жүйелердегі тамаша конверсия мен селективтілікке жақындай алады.[36] П-О лигандтарын хелаттаудан алынған белгілі бір кешендер α, β-қанықпаған кетондар мен эфирлерді гидрлеуде перспективалық нәтижелер көрсетті.[37]
NHC лигандары
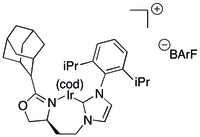
Қарапайым N-гетероциклді карбен (NHC) негізіндегі лигандалар асимметриялық гидрлеу үшін практикалық емес болып шықты.
Кейбір C, N лигандары NHC-ді хирал оксазолинмен біріктіріп, хелаттық лиганд береді.[38][39] Бірінші типтегі NHC негізіндегі лигандтар жеке NHC және оксазолиндердің кішірек кітапханаларының реакциясынан үлкен кітапханалар ретінде пайда болды.[38][39] Функционалсыз олефиндердің каталитикалық гидрогенизациясына иридиумда жеті мүшелі металлоциклді қамтитын NHC негізіндегі катализаторлар қолданылды[38] және винил 80-ші немесе 90-шы жылдардағы эфир спирттері және конверсиялары бар.[40] Сол жүйе бірқатар альдолдарды синтездеуге де қатысты,[41] висинальды диметил[42] және дезоксиполикетид[43] мотивтер мен дезоксиполикетидтердің өздеріне.[44]
C2-симетриялық NHC өздерін асимметриялық гидрлеу үшін өте пайдалы лигандалар ретінде көрсетті.[45]
Ациклді субстраттар
Ациклді қанықпаған субстраттар (олефиндер, кетондар, эминдер елестер ) ең көп таралған прокиральды субстраттарды білдіреді. Асимметриялы гидрогенизацияға әсіресе қолайлы субстраттарда көбінесе гидрленетін учаскеге іргелес полярлы функционалдық топ тән. Бұл функционалды топ болмаған жағдайда, катализ көбінесе төмен энелермен аяқталады. Функционалды емес олефиндер үшін иридий с P,Nнегізделген лигандтар) табысты катализаторларды дәлелдеді. Осы санаттағы катализатордың утилитасы әдеттен тыс тар; Демек, каталитикалық мәселелердің шешілген және шешілмеген көптеген санаттары дамыды. 1,1-бөлінген, 1,2-диарилді три-алмастырылған, 1,1,2-пробиркиль және тетрасубублисентті олефиндер бөлек зерттелген кластарды білдіреді,[46][47] және тіпті осы сыныптар ішінде әртүрлі шешімдерді оңтайлы ететін вариациялар болуы мүмкін.[48]


Олефиндер жағдайына керісінше, эминдердің асимметриялы гидрогенизациясы дифосфин типті лигандаларға қолайлы болды; иридий мен родиумға негізделген жүйелермен тамаша нәтижелерге қол жеткізілді. Алайда, ең жақсы жүйелер де жиі төмен эне мен жалпылықтың жетіспеушілігінен зардап шегеді. Әрине пирролидин - хош иісті кетондардың алынған эминдері катионды родий (I) фосфонит жүйелерімен асимметриялы гидрленуге бейім, ал I2 және сірке қышқылы жүйесі, әдетте ee мәндері 90% -дан жоғары және 99,9% -ке дейін.[49] Осыған ұқсас жүйе иридийді (I) қолданумен және өте тығыз байланысты фосфорамидит лиганд пирролидин типті эминдердің асимметриялы гидрогенизациясы үшін тиімді, олар қос байланыс сақинаның ішінде болған: басқаша айтқанда, дигидропирролдар.[50] Екі жағдайда да, сақина мөлшері бестен алтыға дейін ұлғайтылған кезде энанциоэлектрлік айтарлықтай төмендеді.
Иминдер мен кетондар

Кетондар және елестер байланысты функционалды топтар, және әрқайсысының асимметриялық гидрогенизациясының тиімді технологиялары бір-бірімен тығыз байланысты. Осылардың ішінен Нооридің рутений-хирал дифосфин-диамин жүйесі ең жақсы белгілі жүйелердің бірі болуы мүмкін.[51] Оны фосфиндер мен аминдердің кең спектрімен бірге қолдануға болады (бұл жерде амин болуы мүмкін, бірақ ол қажет емес) және мақсатты субстратпен оңтайлы сәйкестікке оңай реттелуі мүмкін, әдетте энантиомерлі артық (ee's) 90% -дан жоғары.[52][53]
Карбонил және имин субстраттары үшін end1 үйлестіру compete-мен бәсекелесе алады2 режимі. For үшін1-байланысты субстраттар, сутекті қабылдайтын көміртек катализатордан алынады және гидрленуге қарсы тұрады.[54]
Кетондар мен иминдерді асимметриялы гидрлеу үшін, әдетте, иридиум / P, N лиганд негізіндегі жүйелер қолданылады. Мысалы, бензилді арил иминдеріне арналған жүйелі жүйе P, N лиганды SIPHOX-ны иридиймен (I) катиондық кешенде ee> 90% асимметриялық гидрлендіруге қол жеткізу үшін қолданады.[20] Кетондарды асимметриялы гидрогенизациялау үшін қазіргі уақытта дамыған ең тиімді және тиімді катализаторлардың бірі айналым саны (TON) 4 550 000-ға дейін және 99,9% -ке дейін, басқа иридий (I) жүйесін өзара тығыз байланыста қолданады трентат лиганд.[15]

Ұқсастықтарына қарамастан, екі функционалды топ бірдей емес; олар айтарлықтай алшақтайтын көптеген аймақтар бар. Осылардың бірі гидрогенизацияның асимметриялық күйінде болады N-функционалданбаған иминдер, біріншілік аминдер береді. Мұндай түрлерді селективті түрде азайту қиынға соғуы мүмкін, өйткені олар имин мен эминнің күрделі тепе-теңдігінде болады таутомерлер, Сонымен қатар (E) және (З) изомерлер.[55] Бұл мәселеге бір көзқарас қолдану болды кетиминдер олардың гидрохлоридті тұзы ретінде және іргелес алкил немесе стерикалық қасиеттеріне сүйенеді арыл катализаторға екеуін ажыратуға мүмкіндік беретін топтар энантиотопиялық кетиминнің беткейлері.[56][57]
Хош иісті субстраттар
Асимметриялық гидрлеу хош иісті (әсіресе гетероароматикалық ), субстраттар - бұл өте белсенді жүргізіліп жатқан зерттеу аймағы. Бұл саладағы катализаторлар бірқатар күрделі факторларға, соның ішінде гидрогенизацияға төзімділігі жоғары хош иісті қосылыстардың тенденциясына, субстрат пен өнімнің потенциалды үйлестіруші (және сондықтан катализатормен улану) қабілеттеріне, сондай-ақ алмастыру заңдылықтарындағы алуан түрлілікке қарсы тұруы керек. кез-келген хош иісті сақинада болуы мүмкін.[58] Осы субстраттардың ішіндегі ең жақсы жетістік азотты гетероциклдарда байқалды, мұнда хош иісті сақина көбінесе протондау арқылы немесе азоттың одан әрі функционалдануы арқылы (көбінесе электронды шығаратын қорғаныс тобымен) белсендіріледі. Мұндай стратегиялар құрамында оттегі және күкірті бар гетероциклдерге аз қолданылады, өйткені олар негізі де, нуклеофилі де аз; бұл қосымша қиындық олардың асимметриялы гидрогенизациясы үшін неге бірнеше тиімді әдістер бар екенін түсіндіруге көмектеседі.
Хинолиндер, изохинолиндер және хиноксалиндер
2-алмастырылғанды асимметриялық гидрлеу үшін екі жүйе бар хинолиндер оқшауланған кірістілік, әдетте, 80% -дан жоғары, ал ee мәні 90% -дан жоғары. Біріншісі - иридий (I) / хиральфосфин / I2 жүйесі туралы бірінші Чжоу хабарлады т.б.[59] Бұл жүйеде қолданылған алғашқы хиральды фосфин MeOBiPhep болғанымен, жаңа қайталанулар осы лигандтың жұмысын жақсартуға бағытталды. Осы мақсатта жүйелер ауаның тұрақтылығы жақсартылған фосфиндерді (немесе байланысты лигандтарды) пайдаланады,[60] қайта өңделу,[60] дайындалудың қарапайымдылығы,[61] төменгі катализатор жүктемесі[19][62] ахирал фосфин қоспаларының потенциалды рөлі.[63] 2012 жылдың қазан айынан бастап ешқандай механизм ұсынылмаған сияқты, дегенмен екеуі де қажет2 немесе галоген суррогаты және реактивтілікке көмектесудегі гетероароматикалық N-тің мүмкін рөлі туралы құжатталған.[58]
Екіншісі - органокаталитикалық гидрогенизация негізделген жүйе Ханцш эфирлері және хирал Бронстед қышқылы. Бұл жағдайда авторлар изохинолин кезек-кезек протоназаланатын, активтендіретін сатыда болатын механизмді қарастырады, содан кейін Ханцш эфирінен гидридтің конъюгаталық қосылуымен азаяды.[64]

Хиноксалиндердің асимметриялық гидрлеу химиясының көп бөлігі құрылымдық жағынан ұқсас химиямен тығыз байланысты хинолиндер. Тиімді (және тиімді) нәтижелерді Ir (I) / phophinite / I көмегімен алуға болады2 жүйе[65] және Ханцш эфиріне негізделген органокаталитикалық жүйе,[66] екеуі де бұрын қарастырылған жүйелерге ұқсас хинолиндер.
Пиридиндер
Пиридиндер асимметриялық редукция үшін өте өзгермелі субстраттар болып табылады (тіпті басқа гетероароматиктермен салыстырғанда), бастапқы сақинада дифференциалды ауыстыру үшін бес көміртегі орталығы бар. 2012 жылдың қазан айынан бастап, бесеуін басқара алатын ешқандай әдіс жоқ сияқты, дегенмен, кем дегенде бір ақылға қонымды жалпы әдіс бар.
Асимметриялық пиридинді гидрлеудің ең жалпы әдісі іс жүзінде гетерогенді әдіс болып табылады, мұнда асимметрия пиридиннің С2 жағдайына байланысты хирал оксазолидиноннан пайда болады. Осындай функционалданған пиридиндерді әр түрлі гетерогенді метал катализаторларының үстінде гидрогендеу кезінде C3, C4 және C5 позицияларындағы орынбасарлары бар сәйкес пиперидин бар-cis геометрия, жоғары кірістілікте және энансио селективтілікте. Оксазолидинон қосалқы бөлігі гидрлеу жағдайында ыңғайлы түрде бөлінеді.[67]

2-алмастырылған пиридинді гидрогенизациялау үшін арнайы жасалған әдістерге 2-ауыстырылған хинолиндер мен хиноксалиндер сияқты байланысты субстраттар үшін жасалған асимметриялық жүйелер кіруі мүмкін. Мысалы, иридий (I) хиральфосфинІ2 жүйе активтендірілген (алкилденген) 2-пиридинийлерді асимметриялық гидрлеуде тиімді[68] немесе кейбір циклогексанонмен біріктірілген пиридиндер.[69] Сол сияқты, chiral Бронстед қышқылы гидрид көзі ретінде Ханцш эфирімен катализ кейбір 2-алкил пиридиндері үшін қосымша активтендіретін алмастырумен тиімді.[70]
Индолдар
Асимметриялық гидрлеу indoles бастапқыда бағытталған N- қорғалатын индолдар, мұнда қорғайтын топ гетероциклды гидрлендіруге дейін белсендіруге де, металдың екінші координациялық орны ретінде де қызмет ете алады. Кейінгі жұмыс индолды Brønsted қышқылымен белсендіру арқылы қорғалмаған индолдарды бағыттауға мүмкіндік берді.
Ассиметриялық индол гидрлеу туралы есепте, N-ацетил 2-алмастырылған индолдарды жоғары өнімділікпен және 87-95% -бен қорғауға болады. 3-алмастырылған индолдар сәтті болған жоқ, қорғаныш тобының гидролизі индолдың гидрогенизациясынан асып түсті.[71] Ауысу N-тозилді қорғайтын топ гидролиз реакциясын тежеп, 2- және 3-алмастырылған индолдарды гидрогенизациялауға мүмкіндік берді.[72][73] Екі әдіске қатысты мәселе, алайда N-ацетил және N-тозил топтары күрделі субстратпен үйлеспейтін қатаң бөліну жағдайларын талап етеді. Оңай кесілген N-Бок тобы көп ұзамай осындай индолдарды асимметриялы гидрлеудің тиімді әдістері (2 және 3-алмастырылған) дамыды.[74][75]

Қорғалатын индолдарды асимметриялы гидрогенизациялау саласындағы осы жетістіктерге қарамастан, қорғаушы топты толығымен алып тастау арқылы операциялық қарапайымдыққа қол жеткізуге болады. Бұған индолды белсендіру үшін Бронстед қышқылын қолданатын каталитикалық жүйелер қол жеткізді. Бастапқы жүйеде Pd (TFA) қолданылған2/ H8-BINAP жүйесі энанциоселективтіге қол жеткізуге мүмкіндік береді cis- 2,3- және 2-алмастырылған индолдарды гидрогенизациясы, жоғары шығымдылығы және жақсы эе. Осыған ұқсас процесс, мұнда дәйекті Friedel-Crafts алкилденуі және асимметриялық гидрлеу бір кастрюльде жүреді, асимметриялы 2,3-алмастырылған индолиндерді сол сияқты жоғары кірістілікте және ee-де 2 алмастырылған индолдардан іріктеп дайындауға мүмкіндік береді.[76][77]

Перспективалы органокаталитикалық Хираль Льюис негізін қолдана отырып, 2,3-алмастырылған индолдарды асимметриялық гидрлеу әдісі де бар, бірақ бақыланатын э-дер металл негізіндегі гидрогенизациямен бірдей емес.[76]
Пиролес
Толық конверсиясына қол жеткізу пиролдар дейін пирролидиндер ассиметриялы гидрлеу әдісімен гидрогенизация өнімі жиі байқалатын қиын.[78][79] Нәтижесі бастапқы субстратқа да, әдіске де байланысты толық энансиоселективті төмендету мүмкін.
2,3,5-алмастырылған пирролдың асимметриялық гидрогенизациясы мұндай субстраттардың 2 алмастырылған индолдармен бірдей орнын басу схемасына ие екендігін мойындаумен және осы субстраттардың біреуі үшін тиімді болатын асимметриялық гидрлеу жүйесі екеуі үшін де тиімді болуы мүмкін. Мұндай талдау рутений (I) / фосфин / амин базасының 2,3,5-алмастырылған жүйенің дамуына әкелді N-Пирролды алмастырғыштардың табиғатына байланысты дигидро немесе тетрагидропирол (пирролидин) бере алатын пир пиролдары. Барлық фенилді алмастыру схемасы дигидропиролдарға өте жоғары өнімділікке (> 96%) және негізінен мінсіз энансио селективтілікке әкеледі. Толығымен гидрленген, барлығына қол жеткізуcis дигидропирролға диастереоселективті гетерогенді гидрлеу арқылы қол жетімді болуы мүмкін. Алкилді алмастыру дигидроға да, тетрагидропирролға да әкелуі мүмкін, дегенмен өнімділік (> 70%) және энанциоселективтілік (көбінесе> 90%) жоғары болып қалады. The региоселективтілік екі жағдайда да стериктермен басқарылатын сияқты, аз алмастырылған қосарланған гидрогенизацияланған.[78]

Сондай-ақ, қорғалмаған 2,5-пиролды ассиметриялы түрде Brønsted қышқылы / Pd (II) / хиралфосфин-катализденген әдіспен гидрогенизациялауға болады, сәйкесінше 2,5-бөлінген 1-пирролиндер шамамен 70-80% кірістілікте және 80-90% ee.[79]
Құрамында оттегі бар гетероциклдар
Асимметриялық гидрлеу фурандар және бензофурандар осы уақытқа дейін қиын болып шықты.[80] Кейбір Ru-NHC кешені асимметриялық гидрлеуді катализдейді бензофурандар[81] және фурандар.[82] энантиоиндукцияның жоғары деңгейімен.
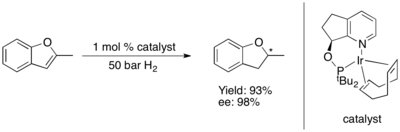
Құрамында күкірт бар гетероциклдер
Құрамында оттегі бар гетероциклдар сияқты, күкірт бастапқы қанықпаған құрамына кіретін қосылыстардың асимметриялы гидрленуі пи-байланыстыру жүйе әзірге шектеулі болып көрінеді тиофендер және бензотиофендер. Осы гетероциклдердің асимметриялық гидрогенизациясының негізгі тәсілі рутений (II) катализаторы мен хирал, C2 симметриялы N-гетероциклді карбен (NHC). Бұл жүйеде керемет таңдамалылық (ee> 90%) және керемет диастереоэлективтілік бар (барлығы) cis) егер субстратта балқытылған (немесе тікелей байланысқан) фенил сақинасы болса, бірақ ол тек өнім береді рацемиялық барлық басқа сыналған жағдайларда өнім.[83]

Гетерогенді катализ
Асимметриялық гидрлеу үшін біртекті емес катализатор коммерцияланған емес.
Алғашқы асимметриялық гидрогенизация жібек тіреуге қойылған палладийге бағытталған. Синхона алкалоидтар энантиоселективті гидрлеу үшін хиральды модификатор ретінде қолданылған.[84]

Белсенді каталитикалық учаскелердің құрылымдық және электрондық қасиеттерін бақылауға мүмкіндік беретін балама әдіс және гетерогенді тіректе біртекті катализ үшін жасалған катализаторлардың иммобилизациясы болып табылады. Катализатордың полимерге немесе басқа қатты тірекке ковалентті байланысы көбінесе жиі кездеседі, дегенмен катализатордың иммобилизациясы арқылы да қол жеткізуге болады. адсорбция бетіне, ион алмасу, немесе тіпті физикалық инкапсуляция. Бұл тәсілдің бір кемшілігі - катализатордың мінез-құлқын өзгертуге, реакцияның энанциоэлектрлік қабілетін төмендетуге тіреудің жақындығының әлеуеті. Бұған жол бермеу үшін катализатор көбінесе тірекпен байланыстырылады, бірақ тіреудің жақын орналасуы катализатордың жұмысын жақсартатын жағдайлар белгілі.[84]
Соңғы тәсіл хиральды және ахиральды органикалық лигандтарды, құрылымдық металл иондарын, каталитикалық белсенді металл иондарын және / немесе алдын-ала құрастырылған каталитикалық белсенді органометалл ядроларын қоса алғанда, әртүрлі компоненттерден хиральды реакция алаңдарын қосатын MOF құрылысын қамтиды.[85] Соның бірі рутений - катализаторлар. Осындай катализаторлардың 0,005 моль% -ның аз бөлігі ғана арил кетондардың асимметриялы гидрогенизациясына қол жеткізуге жеткілікті болды, дегенмен әдеттегі жағдай 0,1 моль% катализаторға ие болды және нәтижесінде энантиомерлі артық 90,6–99,2%.[86]

Өнеркәсіптік қосымшалар

Ноулздің асимметриялық гидрлеу туралы зерттеулері және оны L-Dopa синтезінің өндірістік масштабына қолдану[3] асимметриялық гидрогенизация индустриялық әлемде мықты бастама берді. 2001 жылғы шолу асимметриялы гидрогенизация өндіріс масштабының 50%, пилоттық масштабтың 90% және стендтік шкаланың 74% катализдік, энанциоселективті процестерді құрайтындығын көрсетті, бұл ретте жалпы асимметриялық каталитикалық әдістер әлі де кең қолданылмаған.[87]
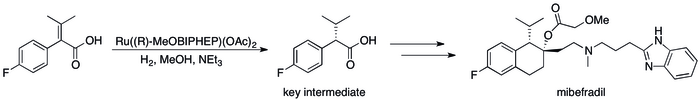
Асимметриялық гидрлеудің өнеркәсіптегі жетістігі[88] кинетикалық ажыратымдылыққа негізделген әдістерді ауыстыру процестің тиімділігін едәуір жақсартуға әкелген бірқатар нақты жағдайлардан байқауға болады. Мысалы, Роштың катализ тобы () синтезіне қол жеткізе алдыS,S) -Ro 67-8867 жалпы кірістіліктің 53% құрайды, бұл шешімді синтезде қол жеткізілген 3,5% -дан жоғары өсім.[89] Роштың синтезі мибефрадил ажыратымдылығын асимметриялық гидрогенизациямен ауыстыру, қадамдар санын үшке азайту және негізгі аралық өнімділікті бастапқы 70% -дан 80% дейін арттыру арқылы жақсартылды.[90]
Әдебиеттер тізімі
- ^ Акабори, С .; Сакурай, С .; Изуми, Ю .; Фудзии, Ю. (1956). «Асимметриялық катализатор». Табиғат. 178 (4528): 323. Бибкод:1956 ж. 178 ж..323А. дои:10.1038 / 178323b0. PMID 13358737. S2CID 4221816.
- ^ а б c Noyori, R. (2003). «Асимметриялық катализ: ғылым және мүмкіндіктер (Нобель дәрісі 2001)». Жетілдірілген синтез және катализ. 345 (12): 15–41. дои:10.1002 / adsc.200390002.
- ^ а б c Ноулз, W. S. (2002). «Асимметриялық гидрогенизация (Нобель дәрісі)». Angewandte Chemie International Edition. 41 (12): 1998–2007. дои:10.1002 / 1521-3773 (20020617) 41:12 <1998 :: AID-ANIE1998> 3.0.CO; 2-8. PMID 19746594.
- ^ Пфальц, А. (2004). «Асимметриялық катализдің арнайы ерекшелігі II бөлім: Асимметриялық катализге арналған хираль лигандтарын жобалау: C-ден2-симметриялық P,P- және N,N- стерикалық және электронды емес симметриялы сызықтар P,N-жарықтар ». Ұлттық ғылым академиясының материалдары. 101 (16): 5723–5726. Бибкод:2004PNAS..101.5723P. дои:10.1073 / pnas.0307152101. PMC 395974. PMID 15069193.
- ^ а б Гриднев, И.Д .; Имамото, Т. (2004). «Rh-катализденген асимметриялық гидрлеу кезіндегі стереоселекция механизмі туралы: энансиоэлектрлік сезімін болжаудың жалпы әдісі». Химиялық зерттеулердің есептері. 37 (9): 633–644. дои:10.1021 / ar030156e. PMID 15379579.
- ^ Ноулз, В.С .; Sabacky, J. J. (1968). «Еритін, оптикалық белсенді, родий кешенін қолданатын каталитикалық асимметриялық гидрлеу». Химиялық байланыс (Лондон) (22): 1445. дои:10.1039 / C19680001445.
- ^ Пилкингтон, С .; Леннон, И. (2003). «Фармацевтикалық аралық өнімдерді өндіру үшін асимметриялық гидрлеуді қолдану: катализатордың алуан түрлілігінің қажеттілігі». Синтез. 2003 (11): 1639. дои:10.1055 / с-2003-40871.
- ^ Мияшита, А .; Ясуда, А .; Такая, Х .; Ториуми, К .; Ито, Т .; Сочи, Т .; Noyori, R. (1980). «2,2'-бис (дифенилфосфино) -1,1'-бинафтил (БИНАП) синтезі, атропизомерлі хирал бис (триарил) фосфин және оны родиумда қолдану (I) -катализденген α- (ациламино) асимметриялық гидрогенизациясы ) акрил қышқылдары ». Американдық химия қоғамының журналы. 102 (27): 7932. дои:10.1021 / ja00547a020.
- ^ Ноори, Р .; Охкума, Т .; Китамура, М .; Такая, Х .; Сайо, Н .; Кумобаяши, Х .; Акутагава, С. (1987). «Β-кето карбондық эфирлерді асимметриялы гидрлеу. Жоғары энантиомерлік тазалықта β-гидрокси эфирлеріне практикалық, таза химиялық қол жетімділік». Американдық химия қоғамының журналы. 109 (19): 5856. дои:10.1021 / ja00253a051.
- ^ Охкума, Такеши; Сандовал, Христиан А .; Шринивасан, Раджагопал; Лин, Квинхонг; Вэй, Иньмао; Муниз, Килиан; Нойори, Риодзи (2005-06-01). «Асимметриялық гидрлеу терт-Алкил кетондар ». Американдық химия қоғамының журналы. 127 (23): 8288–9. дои:10.1021 / ja052071. ISSN 0002-7863. PMID 15941254.
- ^ Охкума, Т .; Хаттори, Т .; Оока, Х .; Иноуэ, Т .; Noyori, R. (2004). «BINAP / 1,4-диамин − рутений (II) кешендері 1-тетралондар мен аналогтарды тиімді асимметриялық гидрогенизациялау үшін». Органикалық хаттар. 6 (16): 2681–2683. дои:10.1021 / ol049157c. PMID 15281743.
- ^ Икария, Т .; Blacker, A. J. (2007). «Кетондарды асимметриялық тасымалдау гидрогенизациясы, екі функционалды өтпелі метал негізіндегі молекулалық катализаторлармен». Химиялық зерттеулердің есептері. 40 (12): 1300–1308. дои:10.1021 / ar700134q. PMID 17960897.
- ^ Шіркеу, Т.Л .; Андерссон, П.Г. (2008). «Олефиндерді дәстүрлі емес функционалды алмастырғыштармен асимметриялық гидрлеудің иридиум катализаторлары». Координациялық химия туралы шолулар. 252 (5–7): 513. дои:10.1016 / j.ccr.2007.09.015.
- ^ а б Лайтфут, А .; Шнидер, П .; Пфальц, А. (1998). «Олефиндерді иранидиум-фосфанодигидрооксазол катализаторларымен энантиоселективті гидрлеу». Angewandte Chemie International Edition. 37 (20): 2897–2899. дои:10.1002 / (SICI) 1521-3773 (19981102) 37:20 <2897 :: AID-ANIE2897> 3.0.CO; 2-8. PMID 29711115.
- ^ а б c Xie, J. H .; Лю, X. Ю .; Xie, JB .; Ванг, Л.Х .; Чжоу, Q. L. (2011). «Қосымша үйлестіру тобы кетондарды асимметриялы гидрлеу үшін өте тиімді хирал иридий катализаторларына әкеледі». Angewandte Chemie International Edition. 50 (32): 7329–32. дои:10.1002 / anie.201102710. PMID 21751315.
- ^ а б c Пфальц, А .; Бланкенштейн, Дж. Р .; Хильграф, Р .; Хорман, Э .; Макинтайр, С .; Менгес, Ф .; Шёнлебер, М .; Смидт, С.П .; Вюстенберг, Б .; Zimmermann, N. (2003). «Олефиндердің иридиум-катализденген энантиоселективті гидрленуі». Жетілдірілген синтез және катализ. 345 (12): 33. дои:10.1002 / adsc.200390027.
- ^ Куй, Х .; Бургесс, К. (2005). «Негізінен жұмыс істемейтін алкендердің каталитикалық біртекті асимметриялық гидрленуі». Химиялық шолулар. 105 (9): 3272–3296. дои:10.1021 / cr0500131. PMID 16159153.
- ^ Xu, Y.; Мингос, Д.М. П .; Браун, Дж. М. (2008). «Crabtree катализаторы қайта қаралды; Лигандтың тұрақтылық пен беріктікке әсері». Химиялық байланыс (2): 199–201. дои:10.1039 / B711979H. PMID 18092086.
- ^ а б Ванг, З. Дж .; Денг, Дж .; Ли, Ю .; Ол, Ю.М .; Танг, В. Дж .; Fan, Q. H. (2007). «Ir катализдейтін хинолиндердің энансио-селективті гидрогенизациясы (BINAP) түсті дендримерлер: каталитикалық белсенділікті күрт күшейту». Органикалық хаттар. 9 (7): 1243–1246. дои:10.1021 / ol0631410. PMID 17328554.
- ^ а б Чжу, С. Ф .; Xie, JB .; Чжан, Ю.З .; Ли, С .; Чжоу, Q. L. (2006). «Жақсы анықталған Chiral Spiro иридиум / фосфин-оксазолин катионды кешендері қоршаған орта қысымында иминдерді жоғары энантиоселективті гидрогенизациялауға арналған». Американдық химия қоғамының журналы. 128 (39): 12886–12891. дои:10.1021 / ja063444p. PMID 17002383.
- ^ а б Блейзер, Х. У .; Пугин, Б. Т .; Шпиндлер, Ф .; Тогни, А. (2002). «Ир дифосфин катализаторларымен имианттардың энансио-селективті гидрогенизациясы: күресу деактивациясы». Comptes Rendus Chimie. 5 (5): 379. дои:10.1016 / S1631-0748 (02) 01391-7.
- ^ Энтальер, С .; Джунге, К .; Beller, M. (2008). «Темірмен тұрақты метал катализі: тоттан бастап, өсіп келе жатқан жұлдызға дейін?». Angewandte Chemie International Edition. 47 (18): 3317–21. дои:10.1002 / anie.200800012. PMID 18412184.
- ^ Михайлин, А .; Лоу, Дж .; Моррис, Р.Х. (2009). «Үлгі синтезі арқылы түзілген құрамында P − N − N − P тетрадентат лиганд бар темір кешені катализдейтін кетондарды тиімді асимметриялық беру гидрогенизациясы». Американдық химия қоғамының журналы. 131 (4): 1394–1395. дои:10.1021 / ja809493h. PMID 19133772.
- ^ Сонненберг, Дж. Ф .; Кумбс, Н .; Дюб, П.А .; Моррис, Р.Х. (2012). «Кетондардың асимметриялық беріліс гидрленуін катализдейтін темір нанобөлшектері». Американдық химия қоғамының журналы. 134 (13): 5893–5899. дои:10.1021 / ja211658t. PMID 22448656.
- ^ Уайтселл, Дж. К. (1989). «C2 симметрия және асимметриялық индукция ». Химиялық шолулар. 89 (7): 1581–1590. дои:10.1021 / cr00097a012.
- ^ Ноулз, В.С .; Сабаки, М. Дж .; Vineyard, B. D. (1972). «Каталитикалық асимметриялық гидрлеу». Химиялық қоғам журналы, Химиялық байланыс (1): 10. дои:10.1039 / C39720000010. PMID 4270504.
- ^ а б Джерфаньон, Т .; Рено, Дж. Л .; Bruneau, C. (2004). «Родий-катализденген асимметриялық гидрлендіруге арналған Chiral монодентатты фосфор лигандары». Тетраэдр: асимметрия. 15 (14): 2101. дои:10.1016 / j.tetasy.2004.04.037.
- ^ Ван Ден Берг, М .; Миннард, А. Дж .; Шудде, Э. П .; Ван Эш, Дж .; Де Вриз, Х.М .; Де Фриз, Дж. Г .; Feringa, B. L. (2000). «Монодентатты лигандтармен жоғары энантиселективті родий-катализденген гидрлеу» (PDF). Американдық химия қоғамының журналы. 122 (46): 11539. дои:10.1021 / ja002507f.
- ^ Фу, Ю .; Xie, J. H .; Ху, А.Г .; Чжоу, Х .; Ванг, Л.Х .; Чжоу, Q. L. (2002). «Родий-катализденетін гидрлеу реакцияларына арналған монодентаттық спиро-фосфор лигандары». Химиялық байланыс (5): 480–481. дои:10.1039 / B109827F. PMID 12120551.
- ^ Reetz, M. T .; Сат, Т .; Мейсвинкель, А .; Мехлер, Г. (2003). «Комбинаторлық асимметриялық өтпелі металдың катализіндегі жаңа принцип: Chiral монодентат P лигандарының қоспалары». Angewandte Chemie International Edition. 42 (7): 790–3. дои:10.1002 / anie.200390209. PMID 12596201.
- ^ Жүзімдік, Б.Д .; Ноулз, В.С .; Сабаки, М. Дж .; Бахман, Г.Л .; Вайнкауф, Дж. (1977). «Асимметриялық гидрлеу. Родий хиральды бисфосфин катализаторы». Американдық химия қоғамының журналы. 99 (18): 5946. дои:10.1021 / ja00460a018.
- ^ Ноулз, В.С .; Сабаки, М. Дж .; Жүзімдік, Б.Д .; Вайнкауф, Дж. (1975). «Родий мен хиральды бисфосфин кешенімен асимметриялық гидрлеу». Американдық химия қоғамының журналы. 97 (9): 2567. дои:10.1021 / ja00842a058.
- ^ Мюллер, Д .; Умбрихт, Г .; Вебер, Б .; Пфальц, А. (1991). «C2-Симметриялы 4,4 ', 5,5'-Тетрагидроби (оксазолдар) және 4,4', 5,5'-Тетрагидро-2,2'-метиленебис [оксазолдар] ретінде Эниантиоселективті катализ үшін алдын-ала байланыс үшін Chiral лигандары ». Helvetica Chimica Acta. 74: 232–240. дои:10.1002 / hlca.19910740123.
- ^ а б Гельмхен, Г.Н .; Пфальц, А. (2000). «ФосфинооксазолиндерӘмбебап, модульдің жаңа класы P,N-Асиметриялық катализге арналған лигандар ». Химиялық зерттеулердің есептері. 33 (6): 336–345. дои:10.1021 / ar9900865. PMID 10891051.
- ^ Францке, А .; Пфальц, А. (2011). «Zwitterionic иридий кешендері P,N-Алкендерді асимметриялы гидрлеудің катализаторы ретіндегі лигандар ». Химия: Еуропалық журнал. 17 (15): 4131–44. дои:10.1002 / химия.201003314. PMID 21381140.
- ^ Маурер, Ф .; Хуч, V .; Ульрих, А .; Казмайер, У. (2012). «Α, β-қанықпаған кетондарды стереоэлектрикалық гидрлеу катализаторларын жасау». Органикалық химия журналы. 77 (11): 5139–5143. дои:10.1021 / jo300246c. PMID 22571628.
- ^ Рейджот, Д .; Woodmansee, D.H .; Пугин, Б. Т .; Пфальц, А. (2011). «Пролин негізіндегі P, O лиганд / иридий комплекстері жоғары селективті катализаторлар: үш алмастырылған алкендерді асимметриялы гидрлеу». Angewandte Chemie International Edition. 50 (41): 9598–601. дои:10.1002 / anie.201104105. PMID 21882320.
- ^ а б c Перри, М. С .; Куй, Х .; Пауэлл, М. Т .; Хоу, Д.Р .; Рибенспилер, Дж. Х .; Бургесс, К. (2003). «Оптикалық белсенді Иридиум Имидазол-2-илиден-оксазолинді кешендер: Арилалкендерді асимметриялы гидрлеуде дайындау және қолдану». Американдық химия қоғамының журналы. 125 (1): 113–123. дои:10.1021 / ja028142b. PMID 12515512.
- ^ а б Нанчен, С .; Пфальц, А. (2006). «Chiral синтезі және қолданылуы N-Гетероциклді карбен - оксазолинді лигандтар: иридиум-катализденген энантиоселективті гидрогенизация ». Химия: Еуропалық журнал. 12 (17): 4550–8. дои:10.1002 / хим.200501500. PMID 16557626.
- ^ Чжу, Ю .; Бургесс, К. (2008). «Винил эфирлерін катализденген иридий-катализденген асимметриялық гидрлеу». Жетілдірілген синтез және катализ. 350 (7–8): 979. дои:10.1002 / adsc.200700546.
- ^ Чжао, Дж .; Бержесс, К. (2009). «Алдол типті широндар, үш алмастырылған алкендердің асимметриялық гидрленуінен». Органикалық хаттар. 11 (10): 2053–2056. дои:10.1021 / ol900308w. PMID 19368378.
- ^ Чжао, Дж .; Берджесс, К. (2009). «Трисубстителген алкендерді асимметриялы гидрлеу әдісімен винальды диметил хирондарының синтезі». Американдық химия қоғамының журналы. 131 (37): 13236–13237. дои:10.1021 / ja905458n. PMID 19719102.
- ^ Чжоу Дж .; Берджесс, К. (2007). «Α, ω-функционалданған 2,4-диметилпентанды диадтар және 2,4,6-триметилептанды триадалар асимметриялық гидрлеу арқылы». Angewandte Chemie International Edition. 46 (7): 1129–31. дои:10.1002 / anie.200603635. PMID 17200966.
- ^ Чжоу Дж .; Чжу, Ю .; Берджесс, К. (2007). «Синтезі (S,R,R,S,R,S) -4,6,8,10,16,18- гексаметилдокозан Antitrogus parvulus Диастереоселективті гидрогенизация арқылы ». Органикалық хаттар. 9 (7): 1391–1393. дои:10.1021 / ol070298z. PMID 17338543.
- ^ Урбан, С .; Ортега, Н .; Glorius, F. (2011). «Ригений катализдейтін хиноксалиндердің лигандпен бақыланатын жоғары региоселективті және асимметриялық гидрленуі N-Гетероциклді карбенді кешендер ». Angewandte Chemie International Edition. 50 (16): 3803–6. дои:10.1002 / anie.201100008. PMID 21442699.
- ^ Пами, О .; Андерссон, П.Г.; Диегес, М. (2010). "Asymmetric Hydrogenation of Minimally Functionalised Terminal Olefins: An Alternative Sustainable and Direct Strategy for Preparing Enantioenriched Hydrocarbons". Химия: Еуропалық журнал. 16 (48): 14232–40. дои:10.1002/chem.201001909. PMID 21140401.
- ^ Woodmansee, D. H.; Pfaltz, A. (2011). "Asymmetric hydrogenation of alkenes lacking coordinating groups". Химиялық байланыс. 47 (28): 7912–7916. дои:10.1039/c1cc11430a. PMID 21556431.
- ^ Mazuela, J.; Verendel, J. J.; Колл, М .; SchäFfner, B. N.; BöRner, A.; Andersson, P. G.; PàMies, O.; DiéGuez, M. (2009). "Iridium Phosphite−Oxazoline Catalysts for the Highly Enantioselective Hydrogenation of Terminal Alkenes". Американдық химия қоғамының журналы. 131 (34): 12344–12353. дои:10.1021/ja904152r. PMID 19658416.
- ^ Hou, G. H.; Xie, J. H.; Wang, L. X.; Zhou, Q. L. (2006). "Highly Efficient Rh(I)-Catalyzed Asymmetric Hydrogenation of Enamines Using Monodente Spiro Phosphonite Ligands". Американдық химия қоғамының журналы. 128 (36): 11774–11775. дои:10.1021/ja0644778. PMID 16953614.
- ^ Hou, G. H.; Xie, J. H.; Yan, P. C.; Zhou, Q. L. (2009). "Iridium-Catalyzed Asymmetric Hydrogenation of Cyclic Enamines". Американдық химия қоғамының журналы. 131 (4): 1366–1367. дои:10.1021/ja808358r. PMID 19132836.
- ^ Охкума, Т .; Ooka, H.; Hashiguchi, S.; Икария, Т .; Noyori, R. (1995). "Practical Enantioselective Hydrogenation of Aromatic Ketones". Американдық химия қоғамының журналы. 117 (9): 2675. дои:10.1021/ja00114a043.
- ^ Ноори, Р .; Ohkuma, T. (2001). "Asymmetric Catalysis by Architectural and Functional Molecular Engineering: Practical Chemo- and Stereoselective Hydrogenation of Ketones". Angewandte Chemie International Edition. 40 (1): 40–73. дои:10.1002/1521-3773(20010105)40:1<40::AID-ANIE40>3.0.CO;2-5. PMID 11169691.
- ^ Hems, W. P.; Groarke, M.; Zanotti-Gerosa, A.; Grasa, G. A. (2007). "[(Bisphosphine) Ru(II) Diamine] Complexes in Asymmetric Hydrogenation: Expanding the Scope of the Diamine Ligand". Химиялық зерттеулердің есептері. 40 (12): 1340–1347. дои:10.1021/ar7000233. PMID 17576143.
- ^ Ноори, Р .; Yamakawa, M.; Hashiguchi, S. (2001). "Metal−Ligand Bifunctional Catalysis: A Nonclassical Mechanism for Asymmetric Hydrogen Transfer between Alcohols and Carbonyl Compounds". Органикалық химия журналы. 66 (24): 7931–7944. дои:10.1021/jo010721w. PMID 11722188.
- ^ Ю, З .; Джин, В .; Jiang, Q. (2012). "Brønsted Acid Activation Strategy in Transition-Metal Catalyzed Asymmetric Hydrogenation of N-Unprotected Imines, Enamines, and N-Heteroaromatic Compounds". Angewandte Chemie International Edition. 51 (25): 6060–72. дои:10.1002/anie.201200963. PMID 22577004.
- ^ Хоу, Г .; Gosselin, F.; Ли, В .; McWilliams, J. C.; Күн, Ю .; Weisel, M.; O'Shea, P. D.; Чен, С .; Davies, I. W.; Zhang, X. (2009). "Enantioselective Hydrogenation of N−H Imines". Американдық химия қоғамының журналы. 131 (29): 9882–9883. дои:10.1021/ja903319r. PMID 19569686.
- ^ Хоу, Г .; Tao, R.; Күн, Ю .; Чжан, Х .; Gosselin, F. (2010). "Iridium−Monodentate Phosphoramidite-Catalyzed Asymmetric Hydrogenation of Substituted Benzophenone N−H Imines". Американдық химия қоғамының журналы. 132 (7): 2124–2125. дои:10.1021/ja909583s. PMID 20104899.
- ^ а б Zhou, Y. G. (2007). "Asymmetric Hydrogenation of Heteroaromatic Compounds". Химиялық зерттеулердің есептері. 40 (12): 1357–1366. CiteSeerX 10.1.1.653.5495. дои:10.1021/ar700094b. PMID 17896823.
- ^ Wang, W. B.; Lu, S. M.; Yang, P. Y.; Han, X. W.; Zhou, Y. G. (2003). "Highly Enantioselective Iridium-Catalyzed Hydrogenation of Heteroaromatic Compounds, Quinolines". Американдық химия қоғамының журналы. 125 (35): 10536–10537. CiteSeerX 10.1.1.651.3119. дои:10.1021/ja0353762. PMID 12940733.
- ^ а б Сю Л .; Lam, K. H.; Джи, Дж .; Ву Дж .; Fan, Q. H.; Lo, W. H.; Chan, A. S. C. (2005). "Air-stable Ir-(P-Phos) complex for highly enantioselective hydrogenation of quinolines and their immobilization in poly(ethylene glycol) dimethyl ether (DMPEG)". Химиялық байланыс (11): 1390–2. дои:10.1039/B416397D. PMID 15756313.
- ^ Lam, K. H.; Сю Л .; Фэн, Л .; Fan, Q. H.; Lam, F. L.; Lo, W. H.; Chan, A. S. C. (2005). "Highly Enantioselective Iridium-Catalyzed Hydrogenation of Quinoline Derivatives Using Chiral Phosphinite H8-BINAPO". Жетілдірілген синтез және катализ. 347 (14): 1755. дои:10.1002/adsc.200505130.
- ^ Qiu, L.; Kwong, F. Y.; Ву Дж .; Lam, W. H.; Чан, С .; Yu, W. Y.; Ли, Ю.М .; Guo, R.; Чжоу, З .; Chan, A. S. C. (2006). "A New Class of Versatile Chiral-Bridged Atropisomeric Diphosphine Ligands: Remarkably Efficient Ligand Syntheses and Their Applications in Highly Enantioselective Hydrogenation Reactions". Американдық химия қоғамының журналы. 128 (17): 5955–5965. дои:10.1021/ja0602694. PMID 16637664.
- ^ Reetz, M. T .; Li, X. (2006). "Asymmetric hydrogenation of quinolines catalyzed by iridium complexes of BINOL-derived diphosphonites". Химиялық байланыс (20): 2159–60. дои:10.1039/b602320g. PMID 16703140.
- ^ Бұзу; Антончик, А .; Theissmann, T. (2006). «Жоғары энансио селективті Бронстед қышқылының катализденетін каскадты реакциясы: хинолиндердің органокаталитикалық трансферттік гидрогенизациясы және оларды алкалоидтар синтезінде қолдану». Angewandte Chemie International Edition ағылшын тілінде. 45 (22): 3683–3686. дои:10.1002 / anie.200600191. PMID 16639754.
- ^ Тан, В .; Сю Л .; Fan, Q. H.; Ванг Дж .; Fan, B.; Чжоу, З .; Lam, K. H.; Chan, A. S. C. (2009). "Asymmetric Hydrogenation of Quinoxalines with Diphosphinite Ligands: A Practical Synthesis of Enantioenriched, Substituted Tetrahydroquinoxalines". Angewandte Chemie International Edition. 48 (48): 9135–8. дои:10.1002/anie.200904518. PMID 19876991.
- ^ Rueping, M.; Tato, F.; Schoepke, F. R. (2010). "The First General, Efficient and Highly Enantioselective Reduction of Quinoxalines and Quinoxalinones". Химия: Еуропалық журнал. 16 (9): 2688–91. дои:10.1002/chem.200902907. PMID 20140920.
- ^ Глориус, Ф .; Spielkamp, N.; Holle, S.; Goddard, R.; Lehmann, C. W. (2004). "Efficient Asymmetric Hydrogenation of Pyridines". Angewandte Chemie International Edition. 43 (21): 2850–2. дои:10.1002/anie.200453942. PMID 15150766.
- ^ Ye, Z. S.; Chen, M. W.; Chen, Q. A.; Ши, Л .; Дуан, Ю .; Zhou, Y. G. (2012). "Iridium-Catalyzed Asymmetric Hydrogenation of Pyridinium Salts". Angewandte Chemie International Edition. 51 (40): 10181–4. дои:10.1002/anie.201205187. PMID 22969060.
- ^ Tang, W. J.; Тан, Дж .; Xu, L. J.; Lam, K. H.; Fan, Q. H.; Chan, A. S. C. (2010). "Highly Enantioselective Hydrogenation of Quinoline and Pyridine Derivatives with Iridium-(P-Phos) Catalyst". Жетілдірілген синтез және катализ. 352 (6): 1055. дои:10.1002/adsc.200900870.
- ^ Rueping, M.; Antonchick, A. P. (2007). "Organocatalytic Enantioselective Reduction of Pyridines". Angewandte Chemie International Edition. 46 (24): 4562–5. дои:10.1002/anie.200701158. PMID 17492817.
- ^ Кувано, Р .; Сато, К .; Kurokawa, T.; Karube, D.; Ito, Y. (2000). "Catalytic Asymmetric Hydrogenation of Heteroaromatic Compounds, Indoles". Американдық химия қоғамының журналы. 122 (31): 7614. дои:10.1021/ja001271c.
- ^ Кувано, Р .; Kaneda, K.; Ито, Т .; Сато, К .; Kurokawa, T.; Ito, Y. (2004). "Highly Enantioselective Synthesis of Chiral 3-Substituted Indolines by Catalytic Asymmetric Hydrogenation of Indoles". Органикалық хаттар. 6 (13): 2213–2215. дои:10.1021/ol049317k. PMID 15200323.
- ^ Кувано, Р .; Kashiwabara, M.; Сато, К .; Ито, Т .; Kaneda, K.; Ito, Y. (2006). "Catalytic asymmetric hydrogenation of indoles using a rhodium complex with a chiral bisphosphine ligand PhTRAP". Тетраэдр: асимметрия. 17 (4): 521. дои:10.1016/j.tetasy.2006.01.016.
- ^ Кувано, Р .; Kashiwabara, M. (2006). "Ruthenium-Catalyzed Asymmetric Hydrogenation of N-Boc-Indoles". Органикалық хаттар. 8 (12): 2653–2655. дои:10.1021/ol061039x. PMID 16737337.
- ^ Baeza, A.; Pfaltz, A. (2010). "Iridium-Catalyzed Asymmetric Hydrogenation of N-Protected Indoles". Химия: Еуропалық журнал. 16 (7): 2036–9. дои:10.1002/chem.200903105. PMID 20104554.
- ^ а б Xiao, Y. C.; Ванг, С .; Яо, Ю .; Сан Дж.; Chen, Y. C. (2011). "Direct Asymmetric Hydrosilylation of Indoles: Combined Lewis Base and Brønsted Acid Activation". Angewandte Chemie International Edition. 50 (45): 10661–4. дои:10.1002/anie.201105341. PMID 21932274.
- ^ Дуан, Ю .; Chen, M. W.; Ye, Z. S.; Wang, D. S.; Chen, Q. A.; Zhou, Y. G. (2011). "An Enantioselective Approach to 2,3-Disubstituted Indolines through Consecutive Brønsted Acid/Pd-Complex-Promoted Tandem Reactions". Химия: Еуропалық журнал. 17 (26): 7193–7. дои:10.1002/chem.201100576. PMID 21567504.
- ^ а б Кувано, Р .; Kashiwabara, M.; Ohsumi, M.; Kusano, H. (2008). "Catalytic Asymmetric Hydrogenation of 2,3,5-Trisubstituted Pyrroles". Американдық химия қоғамының журналы. 130 (3): 808–809. дои:10.1021/ja7102422. PMID 18154340.
- ^ а б Wang, D. S.; Ye, Z. S.; Chen, Q. A.; Zhou, Y. G.; Yu, C. B.; Fan, H. J.; Duan, Y. (2011). "Highly Enantioselective Partial Hydrogenation of Simple Pyrroles: A Facile Access to Chiral 1-Pyrrolines". Американдық химия қоғамының журналы. 133 (23): 8866–8869. дои:10.1021/ja203190t. PMID 21591641.
- ^ Wang, D. S.; Chen, Q. A.; Lu, S. M.; Zhou, Y. G. (2012). "Asymmetric Hydrogenation of Heteroarenes and Arenes". Химиялық шолулар. 112 (4): 2557–2590. дои:10.1021/cr200328h. PMID 22098109.
- ^ Ortega, Nuria; Urban, Slawomir; Beiring, Bernhard; Glorius, Frank (2012). "Ruthenium NHC Catalyzed Highly Asymmetric Hydrogenation of Benzofurans". Angewandte Chemie International Edition. 51 (7): 1710–3. дои:10.1002/anie.201107811. PMID 22311814.
- ^ Wysocki, Jędrzej; Ortega, Nuria; Glorius, Frank (2014). "Asymmetric Hydrogenation of Disubstituted Furans". Angewandte Chemie International Edition. 53 (33): 8751–5. дои:10.1002/anie.201310985. PMID 24554623.
- ^ Урбан, С .; Beiring, B.; Ortega, N.; Пол, Д .; Глориус, Ф. (2012). "Asymmetric Hydrogenation of Thiophenes and Benzothiophenes". Американдық химия қоғамының журналы. 134 (37): 15241–15244. дои:10.1021/ja306622y. PMID 22934527.
- ^ а б Heitbaum, M.; Глориус, Ф .; Escher, I. (2006). «Асимметриялық гетерогенді катализ». Angewandte Chemie International Edition. 45 (29): 4732–62. дои:10.1002 / anie.200504212. PMID 16802397.
- ^ Yoon, M.; Srirambalaji, R.; Kim, K. (2012). "Homochiral Metal–Organic Frameworks for Asymmetric Heterogeneous Catalysis". Химиялық шолулар. 112 (2): 1196–1231. дои:10.1021/cr2003147. PMID 22084838.
- ^ Ху, А .; Ngo, H. L.; Лин, В. (2003). "Chiral Porous Hybrid Solids for Practical Heterogeneous Asymmetric Hydrogenation of Aromatic Ketones". Американдық химия қоғамының журналы. 125 (38): 11490–11491. дои:10.1021/ja0348344. PMID 13129339.
- ^ Blaser, H. U.; Шпиндлер, Ф .; Studer, M. (2001). "Enantioselective catalysis in fine chemicals production". Қолданбалы катализ А: Жалпы. 221 (1–2): 119–143. дои:10.1016/S0926-860X(01)00801-8. PMID 12613584.
- ^ Дуб, Павел А .; Гордон, Джон С. (2018). «Ноери типіндегі молекулалық катализаторлардағы металмен байланысқан N-H функционалдығының рөлі». Nature Reviews Chemistry. 2 (12): 396–408. дои:10.1038 / s41570-018-0049-з. S2CID 106394152.
- ^ Blaser, Hans-Ulrich; Federsel, Hans-Jürgen, eds. (2010). Asymmetric Catalysis on Industrial Scale. Вайнхайм: Вили-ВЧ. 13-16 бет. дои:10.1002/9783527630639. ISBN 978-3-527-63063-9.
- ^ Jacobsen, E.N.; Пфальц, Андреас; Yamamato, H., eds. (1999). Comprehensive Asymmetric Catalysis. Берлин; Нью-Йорк: Спрингер. pp. 1443–1445. ISBN 978-3-540-64336-4.



