Пероксидикарбонат - Peroxydicarbonate
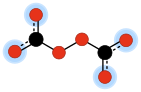
Жылы химия, пероксидикарбонат (кейде пероксодикарбонат) Бұл екі валенталды анион формуламен C
2O2−
6. Бұл бірі оксокарбонды аниондар, тек олардан тұрады көміртегі және оттегі. Оның молекулалық құрылымын екі деп қарастыруға болады карбонат а-ны құрайтын етіп қосылды пероксид көпір –O – O–.
Бірге, анион түзіледі пероксокарбонат CO2−
4, теріс кезінде электрод кезінде электролиз балқытылған литий карбонаты.[1] Анионды судағы қаныққан рубидий карбонат ерітіндісін электролиздеу арқылы да алуға болады.[2]
Сонымен қатар, пероксодикарбонатты анион арқылы алуға болады электросинтез қосулы бор қоспасы бар гауһар (BDD) электродтары. Ресми тотығу карбонатты екі ион анодта өтеді. Пероксодикарбонат анионының жоғары тотығу потенциалына байланысты жоғары анодты асқын потенциал қажет. Бұл одан да маңызды, егер гидроксил радикалдары қалыптастыру процесіне қатысады. Соңғы жарияланым 282 ммоль / л пероксодикарбонат концентрациясына бөлінбеген жасушада жетуге болатындығын көрсетті. натрий карбонаты қазіргі кездегі тығыздығы 720 мА / см² бастапқы материал ретінде[3]. Сипатталған процесс натрий пероксодикарбонатын тәжірибелік түрде өндіруге жарамды.
Калий пероксидикарбонаты Қ2C2O6 арқылы алынған Constam және фон Хансен 1895 жылы;[4] оның кристалдық құрылымы 2002 жылы ғана анықталды.[5] Оны assium20 ° C температурада қаныққан калий карбонат ерітіндісін электролиздеу арқылы алуға болады. Бұл 141 ° C температурада ыдырап, бөлініп шығатын ашық көк кристалды қатты зат оттегі және көмірқышқыл газы, төмен температурада баяу ыдырайды.[5]
Рубидиум пероксодикарбонаты - 424 К (151 ° С) температурада ыдырайтын ашық көк кристалды қатты зат. Оның құрылымы 2003 жылы жарияланған.[2] Екі тұзда да карбонатты екі бірліктің әрқайсысы жазық болады. Ішінде рубидиум Тұтас бүкіл молекула жазық, ал калий тұз екі бірлік әр түрлі және перпендикуляр жазықтықта жатыр, олардың екеуінде де O-O байланысы бар.[2]
Сондай-ақ қараңыз
Әдебиеттер тізімі
- ^ Чен, Ли-Цзян; Лин, Чан-Цзянь; Зуо, Хуан; Ән, Линг-Чун; Хуан, Чао-Мин (2004). «Балқытылған карбонаттағы пероксокарбонат / пероксодикарбонаттың алғашқы спектроскопиялық байқауы». Физикалық химия журналы B. 108 (23): 7553–7556. дои:10.1021 / jp035749l.
- ^ а б c Диннебье, Роберт Е .; Венский, Сашка; Янсен, Мартин (2003). «Рубидиум пероксодикарбонат Rb кристалл және молекулалық құрылымы2[C2O6]". Химия: Еуропалық журнал. 9 (18): 4391–4395. дои:10.1002 / хим.200304914. PMID 14502625.
- ^ Шардон, Хлое П .; Матти, Торстен; Нойбер, Риеке; Фрайда, Матиас; Комнинеллис, Христос (2017-01-23). «DIACHEM® алмазды электродтарды қолдану арқылы пероксодикарбонатты тиімді электрохимиялық өндіріс». Химия. 2 (3): 1037–1040. дои:10.1002 / slct.201601583. ISSN 2365-6549.
- ^ Констам, Э. Дж .; фон Хансен, А. (1896). «Elektrolytische Darstellung einer neuen Klasse oxidierender Substanzen». Zeitschrift für Elektrochemie. 7: 18 фф. дои:10.1002 / bbpc.189600032 (белсенді емес 2020-10-16).CS1 maint: DOI 2020 жылдың қазанындағы жағдай бойынша белсенді емес (сілтеме)
- ^ а б Диннебье, Роберт Е .; Венский, Сашка; Стефенс, Питер В. Янсен, Мартин (2002). «К-тің кристалды құрылымы2[C2O6]". Angewandte Chemie International Edition. 41 (11): 1922–1924. дои:10.1002 / 1521-3773 (20020603) 41:11 <1922 :: AID-ANIE1922> 3.0.CO; 2-T.
| Бұл физикалық химия - қатысты мақала а бұта. Сіз Уикипедияға көмектесе аласыз оны кеңейту. |
