Орто-карборан - Ortho-carborane
 | |
| Атаулар | |
|---|---|
| Басқа атаулар 1,2-дикарбадодекаборан (12), Орто- дикарбадекаборан | |
| Идентификаторлар | |
| EC нөмірі |
|
| Қасиеттері | |
| C2H12B10 | |
| Молярлық масса | 144.22 г · моль−1 |
| Сыртқы түрі | түссіз қатты |
| Еру нүктесі | 320 ° C (608 ° F; 593 K) |
| Қауіпті жағдайлар | |
| GHS пиктограммалары |   |
| GHS сигналдық сөзі | Ескерту |
| H228, H302, H312, H332 | |
| P210, P240, P241, P261, P264, P270, P271, P280, P301 + 312, P302 + 352, P304 + 312, P304 + 340, P312, P322, P330, P363, P370 + 378, P501 | |
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |
| Infobox сілтемелері | |
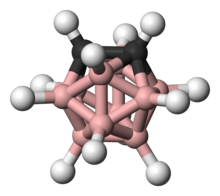
Орто-карборан болып табылады органоборон қосылысы С формуласымен2B10H12. Префикс Орто алынған Орто. Бұл ең көрнекті карборан. Бұл туынды ыстыққа төзімді полимерлерден медициналық қолдануға дейінгі кең ауқымда қарастырылған. Бұл 320 ° С-та ыдырамай еритін түссіз қатты зат.
Дайындық
Клото-дикарбадодекаборанның дайындалуы туралы топтар дербес хабарлады Olin корпорациясы және реактивті қозғалтқыштар бөлімі Thiokol Chemical Corporation астында жұмыс істейді АҚШ әуе күштері Бұл топтар 1,2-клаксо-додекаборанның және онымен байланысты қосылыстардың ауадағы жоғары тұрақтылығын көрсетті, жалпы синтез жасады, алмастырғыштардың карборан кластерін бұзбай трансформациясын сипаттады және мето-изомеризацияға ортоны көрсетті.[1] Кластерде C бар2v симметрия.[2]
Орто-карборан ацетилендер қосу арқылы дайындалады декаборан (14). Заманауи синтездер екі кезеңнен тұрады, біріншісі декаборан қосылысының генерациясын қамтиды:[3][4]
- B10H14 + 2 SE2 → B10H12(SE2)2 + H2
Екінші кезеңде алкин екі көміртегі шыңдарының көзі ретінде орнатылады:[4]
- B10H12(SE2)2 + C2H2 → C2B10H12 + 2 SE2 + H2
Ацетиленнің орнына С-ның қорғалған нұсқалары2H2 ацетилен газына қарағанда ыңғайлы жұмыс істеуге болады:
- B10H12(SE2)2 + C2(CH2O2CCH3)2 → C2B10H10(CH2O2CCH3)2 + 2 SE2 + H2
Органикалық алмастырғыштар тотығу және гидролиз арқылы жойылады:[3]
- 3 C2B10H10(CH2O2CH3)2 + 10 KOH + + 8 KMnO4 → 3 C2B10H12 + 6 CH3CO2K + 8 MnO2 + 6 K2CO3 + 8 H2O
Реакциялар
420 ° C дейін қызған кезде ол мета изомерін түзеді. Пара изомері 600 ° C жоғары температураға дейін қыздыру арқылы алынады.

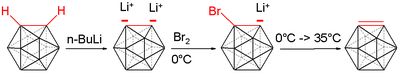
Емдеу органолитий реактивтер дилитио туындысын береді.[5]
- C2B10H12 + 2 BuLi → Li2C2B10H10 + 2 BuH
Бұл сұйылтылған қосылыс әр түрлі электрофилдермен әрекеттеседі, мысалы. хлорофосфиндер, хлорсиланалар және күкірт.[6]
Орто карборанның базалық деградациясы анионды 11-шыңды туынды береді, оның прекурсоры дикарболлид кешендер:[7]
- C2B10H12 + NaOEt + 2 EtOH → Na+C2B9H12− + H2 + B (OEt)3
Дикарболлидтерді қолдану (C2B8H112-) ретінде лигандтарды М. Фредерик Хоторн және оның әріптестері дамытты.[8] Дианион түзіледі сэндвич қосылыстары, бис (дикарболлидтер). Дикарболлидтер күшті электронды донор бола отырып, жоғары тотығу дәрежелерін тұрақтандырады, мысалы. Ni (IV).
орто-карборанды жоғары реактивтіге айналдыруға болады карбиндер В формуласымен10C2H10.
Сондай-ақ қараңыз
Пайдаланылған әдебиеттер
- ^ Хейинг, Т.Л .; Аджер, Дж. В .; Кларк, С.Л .; Мангольд, Дж .; Голдштейн, Х.Л .; Хиллман, М .; Полак, Р. Дж .; Шимански, Дж. В. (1963). «Жаңа органоборан сериясы. I. Декаборанның ацетиленді қосылыстармен реакциясынан карборанес». Бейорганикалық химия. 2 (6): 1089–1092. дои:10.1021 / ic50010a002.
- ^ Дэвидсон, М.Г .; Хибберт, Т.Г .; Ховард, Дж. К .; Макиннон, А .; Уэйд, К. (1996). «Орто, мета және пара-карборандардың кристалды құрылымдары: тек С-H ⋯ O сутегінің гмпаға қосылуымен бағытталатын супрамолекулалық құрылымдар (hmpa = гексаметилфосфорамид)». Хим. Коммун.: 2285–2286. дои:10.1039 / CC9960002285.CS1 maint: авторлар параметрін қолданады (сілтеме)
- ^ а б Чарльз Р. Кутал Дэвид А. Оуэн Ли Дж. Тодд (1968). «closo ‐ 1,2 ‐ Dicarbadodecaborane (12)». Бейорганикалық синтездер. 11: 19–24. дои:10.1002 / 9780470132425.ch5.CS1 maint: авторлар параметрін қолданады (сілтеме)
- ^ а б М. Фредерик Хоторн, Тимоти Д. Эндрюс, Филипп М. Гаррет, Фред П. Олсен, Мартен Рейнтжес, Фред Н. Теббе, Лес Ф. Уоррен, Патрик А. Вегнер, Дональд С. Янг (1967). «Карбаметаллдық бор гидридті туындыларын дайындауға әкелетін икосаэдралды карборандар мен аралық заттар». Бейорганикалық синтездер. 10: 91–118. дои:10.1002 / 9780470132418.ch17.CS1 maint: авторлар параметрін қолданады (сілтеме)
- ^ Попеску, А.-Р .; Мустети, А.Д .; Феррер-Угалде, А .; Виньяс, С .; Нуньес, Р .; Teixidor, F. (2012). «Эфирлік еріткіштің органолитий қосылыстарындағы ықпалды рөлі: карбораниллитий жағдайы». Химия - Еуропалық журнал. 18: 3174–3184. дои:10.1002 / химия.201102626.CS1 maint: авторлар параметрін қолданады (сілтеме)
- ^ Джин, Г.-Х. (2004). «1,2-Dichalcogenolato-o-Carborane Ligands бар органометаллдық кешендер химиясының жетістіктері». Келісім. Хим. Аян. 248: 587–602. дои:10.1016 / j.ccr.2004.01.002.
- ^ Плешек, Дж .; Хеманек, С .; Штибр, Б. (1983). «Калий додекахидро-7,8-дикарба-нидо-некаборатат (1-), k [7,8-C2B9H12], аралық өнімдер, қор ерітіндісі және сусыз тұз ». Бейорганикалық синтездер. 22: 231–234. дои:10.1002 / 9780470132531.ch53.
- ^ Хоторн, М. Ф .; Жас, Д. С .; Вегнер, П.А (1965). «Карбаметаллдық бор гидридті туындылары. I. Ферроцен мен феррикиний ионының айқын аналогтары». Американдық химия қоғамының журналы. 87 (8): 1818–1819. дои:10.1021 / ja01086a053.