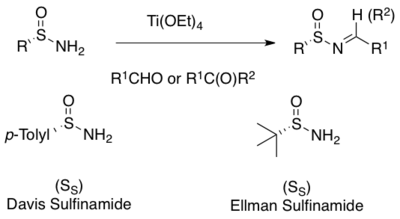
N-сульфинил имині - N-Sulfinyl imine
N-Сульфинил иминдері (N-сульфинлиминдер, сульфиниминдер, тиооксим S-оксидтер) класы болып табылады елестер подшипник а сульфинил азотпен байланысқан топ.[1][2][3][4][5][6][7][8] Бұл суреттер пайдалы көрінеді стереоэлектрлік болуына байланысты реактивтілік хирал электронды алу N-сульфинил тобы. Олар мүмкіндік береді 1,2-қосу туралы металлорганикалық реактивтер елестету. The N-сульфинил тобы стереодезирлеудің күшті және болжамды әсерлерін көрсетеді, нәтижесінде жоғары деңгейлер пайда болады асимметриялық индукция. Расемизация жаңадан құрылған көміртегі-азот стерео-орталықтың алдын алады, өйткені аниондар азотта тұрақталады (яғни, сульфинил тобы аминді қорғаудың жан-жақты тобы). Сульфинил қосалқы хирал қарапайым арқылы оңай жойылады қышқылдық гидролиз. Органометриялық реактивтердің қосылуы N-сульфинил иминдері - бұл симметриялы емес синтездеу үшін ең сенімді және жан-жақты әдіс амин туындылар. Бұл құрылыс блоктары жұмыспен қамтылған асимметриялық синтез көптеген биологиялық белсенді қосылыстар.[1][2][3][4][5][6][7][8]
Синтез
Бірінші N-сульфинил иминдері рацемиялық нысаны туралы хабарлады Франклин А. Дэвис 1974 ж. тотығуымен б-толуол-сулфенил иминдері m-CPBA.[9] Enantiopure б-толуол-сульфинилді кескіндер, М.Синкини және басқалар сипаттаған. 1977 жылы сатылатын Андерсен реактивінің (ментил) реакциясын қосыңыз б-толенсульфинат)[10] металло-кетиминдермен, бірақ алынған кетонмен шектеледі N-сульфинил иминдері.[11] Дайындаудың жалпы әдісі N-сульфинил иминдері - бұл ашираль сульфенил иминдерінің хиральмен асимметриялық тотығуы оксазиридин Дэвис және басқалар хабарлады. 1992 ж.[12] Бұл әдіс хиралды бастауда маңызды рөл атқарды N- сульфинилді иминдер химиясы, оның пайдасы оны дайындау қиындықтарымен шектеледі N-сульфилилоксазиридин.[13] Андерсен реактивінің әр түрлі түрін шығаратын бір кәстрөл процедурасы неғұрлым практикалық болып табылады б-толуол-сульфинилді иминдер хош иісті және алифатты альдегидтерден алынған.[14]
Асимметриялық синтездеу үшін ең кең қолданылатын әдіс N-сульфинил иминдері - энантиопуралық біріншілік сульфинамидтердің альдегидпен немесе кетондармен конденсациясы.[1][2][3][4][5][6][7] Ti (OEt) сияқты сусыздандыратын жұмсақ Льюис қышқылының реактивтері4, сонымен қатар басқа құрғатқыштар / суды тазартқыштар конденсацияны жеңілдетеді.[15][16] Көптеген сульфинамидтер екеуінде де коммерциялық қол жетімді (R)- және (S) құрайды. Ең жиі қолданылатын екеуі - Дэвис б-толуол-сульфинамид және эльман терт-бутансульфинамид[8][15][16]
Қолданбалар
The б-толуол-сульфинилді иминдер α- диастереоселективті асимметриялық синтездеу үшін пайдалыаминқышқылдары,[17][18] β-аминқышқылдары,[19][20] син- және анти-2,3-диаминоэфирлер,[21] α-амин альдегидтері мен кетондары,[22][23] β-аминокетондар,[24][25] α-аминофосфаттар,[26][27] азиридин 2-карбоксилаттар,[28][29] және азиридин 2-фосфонаттар.[30] Осындай көптеген түрлендірулерді терт-бутилсульфинил иминдерімен жүргізуге болады.[8] Аминдердің асимметриялы синтезі үшін литий мен Григнард реактивтері реакцияға түсетіндіктен, терт-бутилсульфинил иминдері қажет. б-толуол-сульфинилді иминдер.[8] Жеңіл қышқылмен емдеу қопсытқыштарды оңай жояды N- бос амин туындыларын беретін сульфинамид өнімдеріндегі -сульфинил тобы. Терт-бутилсулфинил иминдерінің артықшылығы - тиісті сульфинамидтерді қышқылмен өңдеу жанама өнімдерді оңай кетіруге әкеледі[8]
Әдебиеттер тізімі
- ^ а б в Дэвис, Франклин А; Чжоу, Пинг; Чен, Банг-Чи (1998). «Сульфиниминдерді (тиооксим S-оксидтерін) қолдану арқылы амин қышқылдарының асимметриялық синтезі». Химиялық қоғам туралы пікірлер. 27: 13. дои:10.1039 / A827013Z.
- ^ а б в Дэвис, Франклин А; Чжоу, Пинг; Чен, Банг-Чи (2004). «Сульфиниминдерді қолдану арқылы асимметриялық реакциялардың соңғы жетістіктері (N-сульфинил иминдері) ». Тетраэдр. 60: 8003. дои:10.1016 / j.tet.2004.06.071.
- ^ а б в Сенанаяке, Крис Н; Кришнамурти, Дилиепкумар; Луй, Чжи-Хуй; Галлу, I (2005). «Энантиопуралық сульфоксидтер мен сульфинамидтер: олардың стереоселективті синтезіндегі соңғы даму және асимметриялық синтезге қолдану». Aldrichimica Acta. 38: 93. дои:10.1002 / иек.200640264.
- ^ а б в Мортон, Даниел; Стокман, Роберт А (2006). «Chiral рацемиялық емес сульфиниминдер: асимметриялық синтезге арналған жан-жақты реактивтер». Тетраэдр. 62: 8869. дои:10.1016 / j.tet.2006.06.107.
- ^ а б в Дэвис, Франклин А (2006). «Күкірт-азотты химиядағы шытырман оқиғалар». Органикалық химия журналы. 71: 8993. дои:10.1021 / jo061027б.
- ^ а б в Эдупуганти, Рамакришна; Дэвис, Франклин А (2012). «Маскированный оксо-сульфинамидтердің синтезі және асимметриялық синтездегі қолданылуы». Органикалық және биомолекулалық химия. 10: 5021. дои:10.1039 / c2ob25345c.
- ^ а б в Дэвис, Франклин А; Фридман, Артур Дж.; Клюгер, Эдвард В. (1974). «Күкірт-азоттық байланыс химиясы. VIII. N-Алкилиденсульфинамидтер ». Американдық химия қоғамының журналы. 96: 5000. дои:10.1021 / ja00822a055.
- ^ а б в г. e f Эллман, Джонатан; Робак, Мэрянн Т .; Шөп, Мелисса А. (2010). «Терт-бутансульфинамидтің синтезі және қолданылуы». Химиялық шолулар. 110 (6): 3600–740. дои:10.1021 / cr900382t. PMID 20420386.
- ^ Хулс, Мартин; Малломо, Джон П .; Фрай, Лия Л .; Коган, Тимоти Р .; Познер Гэри Н (1990). Органикалық синтез, жинақталған көлем. 7: 495. Жоқ немесе бос
| тақырып =(Көмектесіңдер) - ^ Синкини, Мауро; Козци, Франко (1977). «Оптикалық белсенді синтез N-алкилиденсульфинамидтер ». Химиялық қоғам журналы, Химиялық байланыс: 502. дои:10.1039 / c3977000502b.
- ^ Дэвис, Франклин А .; Редди, Тимма Р .; Редди, Ражараатнам Э. (1992). «Сульфиниминдердің асимметриялы синтезі: несрасемик емес β-аминқышқылдары мен α-гидрокси-β-аминқышқылдарының синтезіне қосымшалар». Органикалық химия журналы. 57: 6387. дои:10.1021 / jo00050a007.
- ^ Дэвис, Франклин А; Редди, Тимма Р .; Хан, Вэй; Кэрролл, П.Дж. (1992). «Оксазиридиндер химиясы. 17. N- (Фенилсулфонил) (3,3-дихлорамфорил) оксазиридин: сульфидті сульфоксидке дейін асимметриялы тотықтыруға арналған өте тиімді реактив ». Американдық химия қоғамының журналы. 114: 1428. дои:10.1021 / ja00030a045.
- ^ Дэвис, Франклин А .; Редди, Раджаратхэм Э .; Cевчик, Джоанна М .; Редди, Г.Венкат; Портоново, Падма С .; Чжан, Хуиминг; Фанелли, декан; Редди, Р.Тимма; Чжоу, Пинг; Кэрролл, Патрик Дж. (1997). «Сульфиниминдердің асимметриялық синтезі және қасиеттері (тиооксим S-оксидтері)». Органикалық химия журналы. 62 (8): 2555–2563. дои:10.1021 / jo970077e. PMID 11671597.
- ^ Лю, Гуанчэн; Коган, Дерек. А .; Оуэнс, Тимоти Д .; Тан, Тони П .; Эллман, Джонатан А. (1999). «Энантиомерлік таза синтез N-терт-бутанесульфинил имидтері (терт-бутанесульфиниминдер) терт-бутансульфинамидтің альдегидтермен және кетондармен тікелей конденсациясы арқылы » Органикалық химия журналы. 64: 1278. дои:10.1021 / jo982059i.
- ^ а б Дэвис, Франклин А .; Чжан Юлиан; Андемайкл, Йемен; Азу, Тянань; Фанелли, Дин Л .; Чжан, Хуиминг (1999). «Enantiopure сульфиниминдерінің (тиооксим S-оксидтері) жақсарған синтезі б-Толуэнсульфинамидтер және альдегидтер мен кетондар ». Органикалық химия журналы. 64: 1403. дои:10.1021 / jo9820622.
- ^ а б Дэвис, Франклин А .; Портоново, Падма С .; Редди, Раджаратнам Е .; Чиу, Ю-Ханг (1996). «Enantiopure сульфиниминдерін және диетилалюминий цианидін қолдану арқылы асимметриялық стрекер синтезі: алкогольге әсер». Органикалық химия журналы. 61: 440. дои:10.1021 / jo9519928.
- ^ Дэвис, Франклин А; Шрираджан, Вайдянатан; Титус, Дональд Д. (1999). «Β-фтор α-аминқышқылдарының тиімді асимметриялық синтезі». Органикалық химия журналы. 64: 6931. дои:10.1021 / jo990947n.
- ^ Дэвис, Франклин А; Редди, Раджаратнам Е .; Шевчик, Джоанна М. (1995). «(S) - (+) - бензилиденнің (R) - (+) - β-фенилаланиннің асимметриялық синтезіб-толуэнсульфинамид. Сульфинимин прекурсорының регенерациясы ». Органикалық химия журналы. 60: 7037. дои:10.1021 / jo00126a070.
- ^ Дэвис, Франклин А; Cевчик, Джоанна М .; Редди, Раджаратнам Е (1996). «(+) - (S) -Этил-β-Амино-3-пиридинепропанаттың эантиопур сульфиниминдерін қолданудың тиімді синтезі». Органикалық химия журналы. 61: 2222. дои:10.1021 / jo951917x.
- ^ Дэвис, Франклин А; Чжан, Янфэн; Qiu, Hui (2007). «Сульфиниминдерді қолданатын анти-және син-2,3-диаминоэфирлердің асимметриялық синтезі. Су және концентрация әсері». Органикалық хаттар. 9: 833. дои:10.1021 / ol063058c. PMC 2533706. PMID 17261004.
- ^ Дэвис, Франклин А .; Рамачандар, Токала; Лю Ху (2004). «Сульфиниминдерден α-амин 1,3-дитиокеталдардың асимметриялық синтезі (N-Сульфинил иминдері). (2S, 3R) - (-) - 3-Hydroxy-3-methylproline синтезі ». Органикалық хаттар. 6: 3393. дои:10.1021 / ol0485971.
- ^ Дэвис, Франклин А; Рамачандар, Токала; Чай, Джин; Скукас, Эдуардас (2006). «Сульфиниминнен α-амин альдегидтерінің асимметриялық синтезі (N-Сульфинил имині) -Диверленген α-Амино 1,3-Дитияндар. (-) - 2,3-транс-3,4-цис-дигидрокси пролинінің формальды синтезі ». Тетраэдр хаттары. 47: 2743. дои:10.1016 / j.tetlet.2006.02.092.
- ^ Дэвис, Франклин А; Нольт, Брэд; Ву, Юнчжун; Прасад, Кавираяни Р .; Ли, Данян; Янг, Бин; Боуэн, Кериша; Ли, Сын Х .; Эардли, Джон Х. (2005). With-амино карбонилді қосылыстардың асимметриялық синтезі N-Сульфинил β-Амино Вайнреб Амидтері ». Органикалық химия журналы. 70: 2184. дои:10.1021 / jo0402780.
- ^ Дэвис, Франклин А; Song Minsoo (2007). «Сульфиниминдер мен Прохираль Вайнреб Амид энолаттарын қолданатын син-α-алмастырылған β-аминокетондардың асимметриялық синтезі». Органикалық хаттар. 9: 2413. дои:10.1021 / ol0708166.
- ^ Дэвис, Франклин А; Ли, Сеун; Ян, Хунксинг; Титус, Дональд Д. (2001). «Сульфиниминдерді қолдана отырып, төрттік α-аминофосфонаттардың асимметриялық синтезі». Органикалық хаттар. 3: 1757. дои:10.1021 / ol015945f.
- ^ Дэвис, Франклин А .; Ли, Сеун; Xu, He (2004). «Оксо сульфинимин маскаларын қолдану арқылы циклді α-аминосфосфонаттардың асимметриялық синтезі (N-Сульфинил иминдері) ». Органикалық химия журналы. 69: 3777. дои:10.1021 / jo040127x.
- ^ Дэвис, Франклин А .; Чжоу, Пинг; Редди, Г.Венкат (1994). «Асимметриялық синтез және реакциялар реакциясыN-(б-Толуэнсульфинил) азиридин-2-карбон қышқылдары ». Органикалық химия журналы. 59: 3243. дои:10.1021 / jo00091a001.
- ^ Дэвис, Франклин А .; Лю, Ху; Чжоу, Пинг; Азу, Тянань; Редди, Г.Венкат; Чжан, Юлиан (1999). «Aza-Darzens асимметриялық синтезі N-б- (Толуэнсульфинил) азиридин 2-Сульфиниминдерден карбоксилат эфирлері (N-Сульфинил иминдері) ». Органикалық химия журналы. 64: 7559. дои:10.1021 / jo990907j.
- ^ Дэвис, Франклин А; МакКоул, Уильям; Титус, Дональд Д. (1999). «Сульфинимин туындысы бар Chiral Enantiopure Aziridinyl-2-фосфонаттарды қолдану арқылы α-метилфосфофенилаланин туындыларының асимметриялық синтезі». Органикалық хаттар. 1: 1053. дои:10.1021 / ol990855k.
- ^ Дэвис, Франклин А .; Ву, Юнчжун; Ян, Хунксинг; МакКоул, Уильям; Прасад, Кавираяни Р. (2003). «Энианопур сульфиниминдерінен азиридин 2-фосфонаттардың асимметриялық синтезі (N-Сульфинил иминдері). Α-амин фосфонаттарының синтезі ». Органикалық химия журналы. 68: 2410. дои:10.1021 / jo020707z.